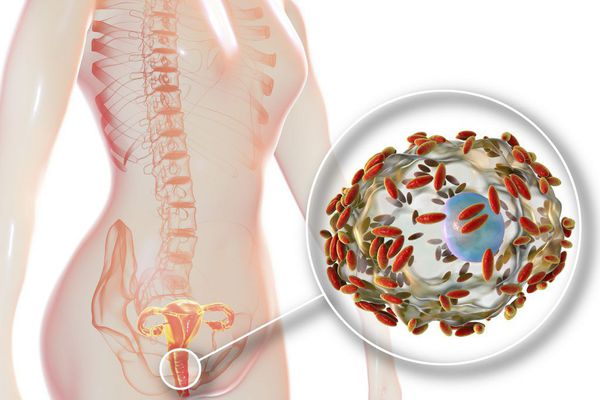
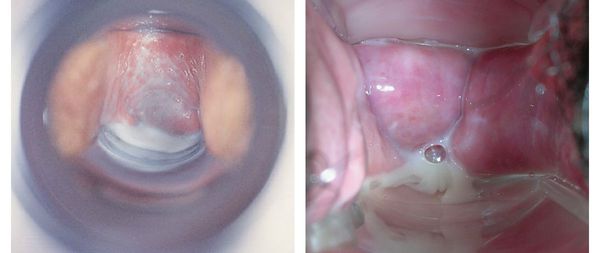
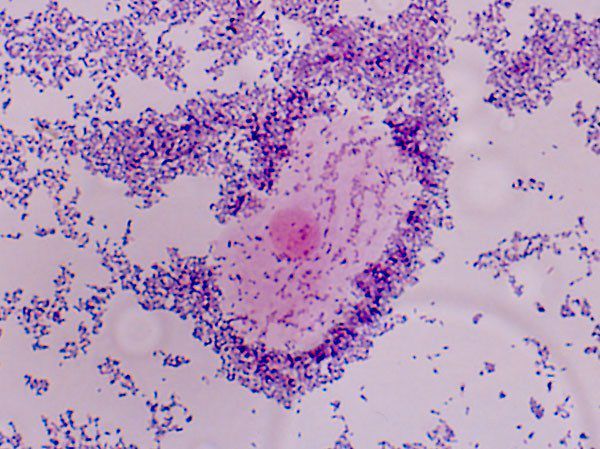
На коже и слизистых оболочках каждого человека обитает разнообразная кокковая флора. Гонококки, пневмококки и другие являются патогенными. Стрептококки и стафилококки, которые представляют большинство данной флоры, считаются условно-патогенными. Эти микроорганизмы присутствуют в небольших количествах и в своих обычных состояниях не вредны для микрофлоры человека. Однако из-за различных неблагоприятных факторов число стрептококков и других микроорганизмов стремительно растет и провоцирует воспалительный процесс.
Симптоматика
Если в мазке у мужчин обнаружено большое количество кокков, могут проявляться такие симптомы:
Но эти признаки характерны не для единичных заболеваниях. Перечисленные симптомы могут быть при уретрите (воспалении мочеиспускательного канала). Поэтому без проведения анализов установить причину воспаления невозможно. Также стоит учесть, что при осложнениях уретрита палочка кокки может находиться в предстательной железе, семенных пузырьках, яичках, а не только в уретре.
Факторы, которые сопутствуют кокобацилярной флоре:
Грамположительные кокки в мазке у мужчин выявляются после передачи инфекции половым путем.
Диагностика заболевания
После обнаружения кокков в мазке у мужчин, необходимо пройти более тщательное обследование и лечение. Если воспаление ярко-выражено, кроме кокобацилярной флоры в поле зрения обнаруживается более 20 лейкоцитов, а также более 10 клеток эпителия.
Мазок, взятый из уретры, исследуют следующими методами:
Как правильно сдавать анализ?
Чтобы получить достоверный результат, необходимо:
Как быстро вылечить заболевание (кокки в мазке у мужчин)?
Если в мазке у мужчин в большом количестве обнаружены полиморфные кокки, необходимо срочно принимать меры. Обратитесь за консультацией и назначением лечения к специалисту, если норма кокков превышена. Помните, что самолечение категорически не рекомендуется.
Что такое бактериальный вагиноз (дисбактериоз влагалища)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Чурсиной Ю.А., гинеколога со стажем в 7 лет.
Определение болезни. Причины заболевания
Бактериальный вагиноз — это инфекционное невоспалительное заболевание, при котором во влагалище происходит обильный рост определённых микроорганизмов и резкое снижение молочнокислых бактерий, обладающих защитными свойствами.
Причины бактериального вагиноза весьма разнообразны. К ним можно отнести как банальные нарушения интимной гигиены, так и более сложные ситуации.
К факторам, влияющим на микрофлору и способствующим возникновению болезни можно отнести:
Возможен ли бактериальный вагиноз у мужчин
Бактериальный вагиноз у мужчин невозможен. Однако мужчина может быть носителем инфекции, которая станет причиной бактериального вагиноза у женщины.
Бактериальный вагиноз у ребёнка
Биоценоз микрофлоры ребёнка формируется при прохождении через родовые пути матери. Если мама — носитель возбудителей бактериального вагиноза, то такая же флора будет и у ребёнка. В таком случае у девочки может развиться бактериальный вагиноз.
Влияние вагиноза на процесс зачатия и на беременность
Бактериальный вагиноз связан со следующими заболеваниями: бесплодие, невынашивание беременности, замершие беременности, преждевременные роды, хориоамнионит (инфицирование оболочек плода и жидкости, окружающих ребёнка в утробе матери) и истмико-цервикальная недостаточность (преждевременное открытие шейки матки при беременности). В основе этих заболеваний лежит хронический эндометрит, возникающий под влиянием возбудителей вагиноза.
Симптомы бактериального вагиноза
Основной признак бактериального вагиноза — это обильные жидкие однородные выделения из половых путей с неприятным запахом. Они могут быть серого или белого цвета.
Чувство жжения и зуда также характерны для вагинита — воспалительного процесса во влагалище. От бактериального вагиноза его отличает чувство сухости влагалища, а также покраснение и отёк его оболочки.
Патогенез бактериального вагиноза
У бактериального вагиноза нет одного конкретного возбудителя — он может быть вызван различными микроорганизмами. К наиболее частым причинам вагиноза относят не только упомянутые G.vaginalis, но и фузобактерии, пептострептококки, вейлонеллу, вагинальный атопобиум, а также бактерии Peptoniphilus, Prevotella, P. bivia и M. Mulieris. Чаще всего развитие болезни провоцирует сочетание 2-3 микроорганизмов и более.
Как передаётся бактериальный вагиноз
Классификация и стадии развития бактериального вагиноза
На данный момент какая-либо классификация и разделение на стадии заболевания отсутствуют. Кода в МКБ-10 (Международной классификации болезней), который бы соответствовал диагнозу «Бактериальный вагиноз», тоже нет. Для кодирования данного состояния используются другие коды. Чаще всего его относят к «N86. Другие воспалительные заболевания влагалища», что является неправильным и не всегда корректным.
Ранее использовалась классификация, предложенная Е.Ф. Кира в 1995 году. Согласно ей, выделяли четыре типа вагинального микробиоценоза — совокупности микроорганизмов, обитающих во влагалище:
Сегодня такая классификация не используется из-за значительного расширения познаний о микробиоценозе влагалища и появлении современных методов лабораторной диагностики.
Классификация бактериального вагиноза на основании микроскопического исследования:
Осложнения бактериального вагиноза
Чем опасен бактериальный вагиноз
Диагностика бактериального вагиноза
Диагностика бактериального вагиноза обычно не представляет существенных трудностей. Тем не менее при постановке диагноза часто можно встретить ошибки: как гипердиагностику (когда пациентке приписывается болезнь, которой у неё на самом деле нет), так и гиподиагностику.
Чаще всего правильно определить заболевание удаётся уже при первом обращении женщины к врачу. В таких случаях диагноз ставится на основании характерных жалоб, данных осмотра и Рh-метрии влагалищных выделений. Иногда может понадобится достаточно обширное клинико-лабораторное обследование.
Какие показатели важны для диагностики бактериального вагиноза
В диагностике бактериального вагиноза используются критерии R. Amsel. К ним относятся:
Диагноз «Бактериальный вагиноз» устанавливается при наличии минимум трёх признаков.
Также существует полуколичественная оценка мазков влагалищной жидкости, окрашенных по Граму, по шкале от 0 до 10. Сейчас этот метод практически не используется.
Для лабораторной диагностики бактериального вагиноза применяется метод PCR Real Time в рамках комплексного анализа микрофлоры влагалища. Существует ряд тест-систем, самыми распространёнными из которых являются Фемофлор 16+КВМ и Фемофлор скрин. Данные тест-системы позволяют получить достаточно полное представление об особенностях микробиоценоза влагалища женщины и назначить обоснованное лечение.
К клиническим методам диагностики относят различные экспресс-тесты: Fem-exam, BVBlue, Pip-activity TestCard. Однако все они диагностики широко не применяются в клинической практике. В основном это связано с их недостаточной чувствительностью.
Дифференциальная диагностика с трихомониазом, кандидозом и уреаплазмозом
Лечение бактериального вагиноза
К какому врачу обратиться
Лечением бактериального вагиноза занимается гинеколог.
Когда стоит обратиться к врачу
К врачу следует обратиться при появлении симптомов бактериального вагиноза: обильных выделениях из половых путей с неприятным запахом, зуде или жжении во влагалище и в области прямой кишки, нарушении мочеиспускания и болезненных ощущениях во время или после полового акта.
Как лечить вагиноз дома. Народные средства от бактериального вагиноза
Ни в коем случае нельзя заниматься самолечением — его должен назначать врач, иначе это может негативно сказаться на здоровье женщины.
Чем лечить бактериальный вагиноз
Для устранения бактериального вагиноза используют антисептические средства и различные комбинированные препараты. В настоящее время доказана эффективность двухэтапной схемы лечения бактериального вагиноза: первый этап заключается в применении антисептических средств, а второй — в восстановлении микрофлоры влагалища.
Существует достаточно много как зарубежных, так и российских рекомендаций и схем лечения данного заболевания. В соответствии с Евразийскими клиническими рекомендациями по рациональному применению антимикробных средств в амбулаторной практике, при устранении бактериального вагиноза следует использовать следующие препараты [7] :
Средства терапии первой линии:
Средства терапии второй линии:
Продолжительность и кратность приёма этих средств определяется врачом индивидуально. Кроме того, существует значительное количество комбинированных препаратов.
Эубиотики (пробиотики)
Для восстановления вагинальной микрофлоры могут быть использованы вагинальные капсулы с живыми лактобактериями и гель с молочной кислотой.
Особенности лечения у беременных
В первом триместре беременности не применяют препараты системного действия. Лечение проводят только местно, свечами, например «Клиндацином». Со второго-третьего триместра, помимо местного лечения, можно применять метронидазол и клиндамицин в таблетках.
Питание при бактериальном вагинозе
Соблюдение диеты на течение бактериального вагиноза не влияет. При лечении следует исключить алкоголь, так как применяемые препараты могут замедлить расщепление этилового спирта, в результате чего общее самочувствие ухудшится.
Прогноз. Профилактика
Прогноз при своевременно начатом лечении в большинстве случаев благоприятный. Иногда возможны рецидивы заболевания. При их возникновении необходим комплексный подход к пациентке, полное клинико-лабораторное обследование и исключение сопутствующих заболеваний, которые могут увеличивать риск повторного появления бактериального вагиноза. Также нужно проконсультироваться по вопросам питания и образа жизни.
В качестве профилактики возникновения бактериального вагиноза прежде всего нужно исключить такие факторы риска, как:
Существенный вклад в развитие и рецидивы заболевания вносят частые смены половых партнёров, тяжёлые сопутствующие заболевания, злоупотребление алкоголем, курение. Всего этого следует избегать.
Немаловажную роль в профилактике играет здоровый образ жизни, адекватная физическая активность и приверженность к правильному питанию — вегетарианская диета и повышенное потребление «быстрых» углеводов увеличивают риск рецидива.
Для предупреждения бактериального вагиноза нужно следовать рекомендациям по интимной гигиене:
Можно ли заниматься сексом при бактериальном вагинозе
Заниматься сексом при бактериальном вагинозе можно, так как он не относится к заболеваниям, передающимся половым путём. Однако бактериальный вагиноз ассоциирован с уреаплазмозом и микоплазмозом, поэтому клинические проявления могут возникнуть и у сексуального партнёра заражённой женщины. Кроме того, бактериальный вагиноз зачастую сопровождается характерным «рыбным» запахом и обильными выделениями, что может стать психологической преградой для полового акта.
Микрофлора урогенитального тракта у мужчин, обследованных по поводу хронического простатита
Лечение хронической воспалительной патологии урогенитального тракта у мужчин всегда было непростой задачей в урологии. Лечение по поводу этих заболеваний, особенно осложненных нарушением фертильности, сексуальной дисфункцией, синдромом тазовых болей, может быть успешным, если производится индивидуально и базируется на знании этиологии воспалительного процесса, иммунореактивности на данный воспалительный процесс и морфо-функциональные изменений в тазовых органах.
В широкой врачебной практике в настоящее время при диагностике этиологического фактора воспалительной патологии урогенитального тракта акцент делается на выявление инфекций передаваемых половым путем. Целью данного исследования является демонстрация значимости других, не менее важных, этиологических факторов, а также места ИППП в патогенезе данной группы воспалительных заболеваний. Инфекционный воспалительный процесс в урогенитальном тракте возникает по двум механизмам.
В первом случае вирулентная ИППП вызывает клинически и лабораторно идентифицируемый уретрит, который в дальнейшем приводит к возникновению восходящего воспалительного процесса. Патогенетическая роль инфекции передаваемой половым путем в данном случае очевидна: при исследовании отделяемого из уретры, секрета предстательной железы, семенной жидкости выявляется достоверное увеличение количества лейкоцитов и ИППП; первично воспалительный процесс начинается с клиники уретрита. Пациенты с воспалительным процессом такого характера чаще всего находятся на лечении в кожно-венерологических диспансерах, когда помимо острого венерического заболевания имеется клиника простатита.
Второй механизм более сложный. Возникновению инфекционного воспалительного процесса в урогенитальном тракте в данном случае предшествуют определенные предрасполагающие факторы.
Выделим несколько основных групп:
При развитии инфекционного процесса в урогенитальном тракте по данному механизму отсутствует какая-либо клиника уретрита, в исследованиях отделяемого из уретры будет отсутствовать достоверное увеличение количества лейкоцитов, в соскобах из уретры будет значительно реже выявляться ИППП, однако у пациентов будет присутствовать клинически и лабораторно идентифицируемый воспалительный процесс в простато-везикулярном комплексе или в органах мошонки.
При наличии вышеуказанных предрасполагающих факторов инфицирование урогенитального тракта банальной бактериальной микрофлорой принципиально возможно двумя путями: трансуретральным и гематогенным.
Гематогенным путем инфицирование чаще всего происходит из очагов хронической инфекции при сопутствующей ЛОР- патологии, заболеваниях, имеющих широчайшее распространение у населения; при заболеваниях прямой кишки с хроническими запорами, геморрое ( особенно при частых обострениях). Инфицирование по данному пути чаще всего происходит тогда, когда в предстательной железе уже имеются выраженные структурные изменения ( конгестия, кальцинаты, ДГПЖ ).
Более значим трансуретральный путь инфицирования вторичной бактериальной микрофлорой.Следует выделить 4 основных источника бактериального инфицирования.
Таблица микроорганизмов, наиболее часто встречающихся в половых органах у женщин при воспалительных заболеваниях, вызванных влагалищной гарднареллой и неспорообразующими бактериями. ( сборник трудов УрНИИДВиИ, 1985 год )
Виды микроорганизмов.
Морфологические особенности.
Коккобациллы одиночные, парные, полиморфные
Современные подходы к терапии хронического бактериального простатита
Хронический простатит (ХП) принадлежит к числу самых распространенных урологических заболеваний. По данным Н. А. Лопаткина (1998), в России на долю ХП приходится до 35% всех обращений к врачу по поводу
Хронический простатит (ХП) принадлежит к числу самых распространенных урологических заболеваний. По данным Н. А. Лопаткина (1998), в России на долю ХП приходится до 35% всех обращений к врачу по поводу урологических проблем среди мужчин в возрасте от 20 до 50 лет. Для получения данных о частоте встречаемости симптомов простатита с оценкой распространенности дизурии, дискомфорта в промежности и в области полового члена было проведено международное (Англия, Франция, Голландия, Корея) эпидемиологическое исследование Urepik. Анализ, проводившийся на основании шкалы симптомов Nickel и Sorensen (1996), дал возможность выявить признаки простатита у 4800 мужчин в возрасте от 40 до 79 лет. У 35% мужчин за последний год наблюдался как минимум один из симптомов простатита, и для 8% мужчин это представляло, по меньшей мере, неудобство [1].
На долю хронического бактериального простатита (ХБП) приходится 5–15% случаев заболевания [6]. Наиболее распространенными, по мнению большинства исследователей, этиологическими агентами ХБП являются такие грамотрицательные бактерии семейства Enterobacteriaceae, как Escherichia coli, которые обнаруживаются в 65–80% случаев инфекций. Различные виды Serratia, Klebsiella, Enterobacter, Acinetobacter выявляются у 10–15% больных. Большинство исследователей полагают, что на долю таких грамположительных бактерий, как Enterococcus faecalis, приходится от 5 до 10% случаев подтвержденных инфекций простаты [5].
В настоящее время обсуждается роль грамположительных бактерий — коагулазо-негативных стафилококков и стрептококков в развитии ХБП [5, 6, 7]. По нашим данным (Е. Б. Мазо и соавт., 2003, 2004) [1], основанным на результатах микробиологического исследования, которое проводилось в виде четырехстаканного теста Meares–Stamey у 70 больных с ХБП с 2002 г., именно коагулазо-негативные стафилококки играют ведущую роль (66%), если говорить об этиологии ХБП. Между тем на долю грамотрицательных патогенов приходится 19% случаев ХБП, а 15% составляют больные с Enterococcus faecalis. Аналогичными данными располагают М. Ф. Трапезникова и соавторы (2004), суммировавшие результаты идентификации 662 штаммов микроорганизмов у 264 больных ХБП, за которыми велось наблюдение в течение последних 13 лет. При этом выявлена ведущая роль грамположительных кокков в этиологии ХБП: за последние 3 года частота распространения коагулазо-негативных стафилококков составила 87,5% [3]. В то же время удельный вес грамотрицательных палочек — «общепризнанных» возбудителей ХБП — за предыдущие 7 лет неуклонно снижался (с 13,3 до 4,2%). С. Н. Калинина, В. П. Александров, О. Л. Тиктинский (2003) при обследовании 174 больных ХБП также выявили преобладание (82%) грамположительной флоры. Инфекция простаты может быть следствием бактериальной колонизации мочеиспускательного канала. Нормальная флора мочеиспускательного канала у мужчин состоит главным образом из дифтероидов и грамположительных кокков. Сексуальная активность может способствовать колонизации мочеиспускательного канала потенциальными уропатогенами. Blacklock (1974) и Stamey (1980) отметили, что секрет простаты у некоторых мужчин с ХБП содержал те же уропатогены, которые присутствовали в вагинальной флоре их сексуальных партнерш. Бактериальная колонизация может также вызвать персистенцию бактерий в простате. Отличительной чертой этого состояния является персистенция бактерий внутри простаты, несмотря на лечение антибиотиками, что связано с хроническим воспалением и склонностью к обострению инфекции мочевыводящего тракта тем же самым патогеном.
К предрасполагающим факторам развития ХБП относятся: уретропростатический рефлюкс; фимоз; анально-генитальные сношения без предохранения; инфекции мочевых путей; острый эпидидимит; постоянные уретральные катетеры и проведение трансуретральных операций у мужчин с инфицированной мочой без предшествующей антимикробной терапии [1]. У пациентов с ХП может быть выявлено нарушение секреторной функции простаты, характеризующееся изменением состава секрета, т. е. снижением уровней фруктозы, лимонной кислоты, кислой фосфатазы, катионов цинка, магния и кальция; цинксодержащего антибактериального фактора простаты. При этом увеличиваются такие показатели, как рН, отношения изоферментов лактатдегидрогеназы-5 к лактатдегидрогеназе-1, белков воспаления — церулоплазмина и компонента комплемента С3. Эти изменения в секреторной функции простаты также обусловливают неблагоприятное воздействие на антибактериальную природу секрета простаты. Уменьшение действия антибактериального фактора простаты способно снижать врожденную противобактериальную активность секрета, тогда как щелочной показатель рН может препятствовать диффузии в ткань и в секрет простаты основных антимикробных препаратов.
Симптомами ХП являются боли в тазовой области, расстройства мочеиспускания и эякуляции (см. табл. 1).
| Таблица 1 Симптомы хронического простатита | ||
| Локализация боли в тазовой области | Расстройство мочеиспускания | Расстройство эякуляции |
| В промежности В половом члене В яичках В паховой области Над лоном В прямой кишке В крестце | Учащенное мочеиспускание Неполное опорожнение мочевого пузыря Слабая или прерывистая струя мочи Боль или ее усиление во время мочеиспускания | Боли во время или после эякуляции Гемоспермия |
Ведущее место в лабораторной диагностике ХБП принадлежит микробиологическому исследованию — четырехстаканному локализационному тесту, предложенному в 1968 г. Meares и Stamey [8]. Он состоит в получении, после тщательного туалета наружных половых органов (во избежание контаминации поверхностными бактериями), первой (10 мл) и второй (средней) порций мочи для бактериологического исследования, массажа предстательной железы (ПЖ) со взятием секрета для микроскопии и посева, а также третьей порции мочи (после взятия секрета) для посева (рис. 1). Количественные посевы первой и второй порций мочи выявляют бактерии в уретре и мочевом пузыре, в то время как при посевах секрета простаты и порции мочи после взятия секрета (третьей порции мочи) выявляют флору простаты. ХБП характеризуется воспалительной реакцией в секрете (при микроскопии определяется более 10 лейкоцитов в поле зрения при большом увеличении). После инкубации посевов подсчитывают количество колониеобразующих единиц (КОЕ).
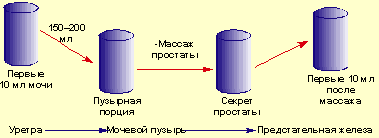 |
| Рисунок 1. Четырехстаканный локализационный тест Meares–Stamey |
Бактериологическое подтверждение ХБП мы проводим на основании, по крайней мере, одного из следующих критериев, предложенных K. G. Naber (2003):
Характерное для ХБП содержание патогенов в образцах примерно следующее:
первая порция мочи 3 КОЕ/мл;
вторая порция мочи 3 КОЕ/мл;
секрет простаты ≥ 10 4 КОЕ/мл;
третья порция мочи ≥ 10 3 КОЕ/мл.
Четкое соблюдение правил микробиологической диагностики и вышеуказанных критериев интерпретации результатов локализационного теста Meares — Stamey на большом количестве наблюдений позволят более точно определить частоту встречаемости истинных патогенов ХБП.
Антимикробная терапия. После идентификации этиологического агента и определения антибиотикорезистентности возникает необходимость назначения больному с ХБП антимикробной терапии. К факторам, оказывающим влияние на выбор антимикробного препарата для лечения ХБП, относятся: чувствительность идентифицированного микроорганизма к антибиотику, его способность в достаточной концентрации проникать через гематопростатический барьер и накапливаться в ткани и секрете простаты, сперме, а также способность препарата преодолевать экстрацеллюлярную полисахаридную оболочку, формируемую микроколониями бактерий, и хорошая переносимость при длительном пероральном приеме. Идеальный антибактериальный препарат для лечения ХБП должен быть жирорастворимым, слабощелочным, с коэффициентом диссоциации, способствующим максимальной концентрации препарата в простате [2]. Антимикробные средства из группы фторхинолонов на сегодняшний день отвечают вышеперечисленным требованиям и являются препаратами выбора для лечения ХБП. Особенностью антибактериального действия фторхинолонов является наличие двух мишеней действия в бактериальной клетке, каковыми являются ферменты (топоизомеразы II типа), ответственные за изменения пространственной конфигурации бактериальной ДНК: ДНК-гираза и топоизомераза IV. ДНК-гираза осуществляет суперспирализацию бактериальной ДНК, а топоизомераза IV — разделение дочерних хромосом в процессе репликации. Ключевым моментом в действии фторхинолонов является образование трехкомпонентного комплекса (бактериальная ДНК–фермент–фторхинолон). Указанный комплекс предотвращает репликацию бактериальной ДНК. Благодаря тому, что топоизомеразы обладают расщепляющей активностью, происходит разрушение молекулы ДНК (С. В. Сидоренко, 2002).
 |
| Рисунок 2. Классификация фторхинолонов (по K.G. Naber,1998) |
В настоящее время в практическое здравоохранение внедрены новые антимикробные препараты из группы фторхинолонов III и IV поколений, которые проявляют активность в отношении как грамотрицательных и грамположительных бактерий, так и атипичных внутриклеточных микроорганизмов, а также обладают способностью воздействовать на бактерии в биологических пленках (см. рис. 2). Антимикробная активность in vitro фторхинолонов III поколения — спарфлоксацина и левофлоксацина, а также фторхинолона IV поколения — моксифлоксацина наглядно представлена в таблице 2.
| Таблица 2 Антимикробная активность in vitro спарфлоксацина, левофлоксацина и моксифлоксацина (МПК90, мкг/мл) [4] | |||
| Микроорганизмы | Спарфлоксацин | Левофлоксацин | Моксифлоксацин |
| Acinetobacter spp. | 0,25 | 16 | 0,5 |
| Citrobacter freundii | 0,25 | 0,5 | 0,5 |
| Enterobacter cloacae | 0,5 | 0,5 | 0,5 |
| Escherichia coli | 0,12 | 0,12 | 0,5 |
| Klebsiella pneumoniae | 0,25 | 0,25 | 0,5 |
| Proteus mirabilis | 0,5 | 0,25 | 0,12 |
| Pseudomonas aeruginosa | 8 | 4 | 16 |
| Staphylococcus epidermidis | 1 | 1 | 2 |
| Staphylococcus saprophyticus | 0,25 | — | 0,5 |
| Enterococcus faecalis | 2 | 16 | 4 |
В 2004 г. мы сравнили чувствительность 25 различных штаммов коагулазо-негативных стафилококков — наиболее распространенных, по нашим данным (Е. Б. Мазо и соавт., 2003, 2004), этиологических агентов ХБП — к левофлоксацину, спарфлоксацину и моксифлоксацину. Бактериологическое исследование проводили классическим методом: выполняли посев мочи и секрета простаты на питательные среды с выделением чистой культуры и идентификацией выделенных штаммов при помощи полуавтоматического микробиологического анализатора Sceptor (Becton Dickinson, USA). Чувствительность выделенных микроорганизмов к левофлоксацину, спарфлоксацину и моксифлоксацину определяли дискодиффузионным методом на среде Мюллера–Хинтона. Результаты оценивали по значениям диаметров зон задержки роста. Всего было изучено 25 штаммов коагулазо-негативных стафилококков (21 — Staphylococcus haemolyticus, 3 — Staphylococcus epidermidis, 1 — Staphylococcus warnerii), выделенных в диагностическом титре из секрета простаты и мочи у больных ХБП при четырехстаканном тесте Meares–Stamey. Проведенный нами анализ чувствительности коагулазо-негативных стафилококков к фторхинолонам III и IV поколений показал наиболее высокую чувствительность этих бактерий к моксифлоксацину — у 24 (96%) штаммов. К левофлоксацину оказались чувствительны 21 (84%), а к спарфлоксацину 20 (80%) штаммов коагулазо-негативных стафилококков. Пять резистентных к спарфлоксацину штаммов были выделены нами у больных после длительной антимикробной терапии этим препаратом. Был выделен также штамм гемолитического стафилококка, резистентный ко всем фторхинолонам III и IV поколений у больного, ранее принимавшего в течение 6 нед моксифлоксацин. Проведенное исследование продемонстрировало высокую чувствительность коагулазо-негативных стафилококков, выделенных от больных ХБП, к фторхинолонам III и IV поколений. Чувствительность исследованных бактерий к моксифлоксацину оказалась наиболее высокой, в то время как к левофлоксацину и спарфлоксацину была практически одинаково ниже. Таким образом, длительная антимикробная терапия моксифлоксацином может привести к селекции устойчивых штаммов и развитию перекрестной резистентности к фторхинолонам III и IV поколений.
На сегодняшний день проведено ограниченное количество клинических исследований применения фторхинолонов в лечении ХБП. Результаты таких исследований, с периодом наблюдения не менее 6 мес, представлены в таблице 3.
Как видно из данных, приведенных в таблице 3, несмотря на существенные различия в количестве больных, принимавших участие в исследованиях, бактериальная эрадикация при различной длительности терапии фторхинолонами, наблюдалась более чем у 60% пациентов. Проведение подобных исследований в будущем, с соблюдением стандартов микробиологической диагностики, позволит выработать единый подход к рациональной антимикробной терапии ХБП.
Согласно актуальным на сегодняшний день рекомендациям Европейской ассоциации урологов по лечению инфекций мочевыводящих путей и инфекций репродуктивной системы у мужчин, принятым в 2001 г., длительность антимикробной терапии ХБП фторхинолонами или триметопримом должна составлять 2 нед (после установления предварительного диагноза). После повторного обследования больного антимикробную терапию рекомендуют продолжать суммарно в течение 4–6 нед только при положительном результате микробиологического исследования секрета простаты, взятого до начала лечения, или в случае, если у больного улучшилось состояние после приема антимикробных препаратов [2].
Антимикробные препараты, используемые для лечения ХБП, а также способы их применения приведены в таблице 4.
| Таблица 4 Способы применения антимикробных препаратов для лечения хронического бактериального простатита | ||
| Группа препаратов | Препараты | Способ применения |
| Фторхинолоны | Ципрофлоксацин (сифлокс, ципролет, цифран) | По 500 мг 2 раза в сутки |
| Офлоксацин (джеофлокс, заноцин, офлоксин 200) | По 400 мг 2 раза в сутки | |
| Ломефлоксацин (ксенаквин, ломфлокс, максаквин) | По 400 мг 1 раз в сутки | |
| Левофлоксацин (таваник) | По 500 мг 1 раз в сутки | |
| Спарфлоксацин (спарфло) | Первый прием 400 мг, затем по 200 мг 1 раз в сутки | |
| Моксифлоксацин (авелокс) | По 400 мг 1 раз в сутки | |
| Триметоприм/ сульфаметоксазол | Ко-тримоксазол (бикотрим, бисептол) | По 960 мг 2 раза в сутки |
Следует отметить, что больные с ХБП должны принимать антибиотик фторхинолонового ряда в течение длительного периода (от 4 до 6 нед) для предотвращения рецидива инфекции нижних мочевых путей. Продолжительная терапия антибиотиками в низких профилактических дозах или супрессивная антимикробная терапия могут применяться в случаях рецидивирующего или невосприимчивого к лечению простатита.
Литература
С. В. Попов
А. К. Чепуров, доктор медицинских наук, профессор
В. И. Карабак, кандидат медицинских наук
РГМУ, Москва