Силикоз
Силикоз – профзаболевание, характеризующееся развитием тяжелого пневмофиброза вследствие продолжительного вдыхания пыли с высоким содержанием свободной двуокиси кремния. Симптоматика носит прогрессирующий характер: одышка сначала возникает при нагрузке, затем и в покое, периодическое покашливание сменяется постоянным кашлем, усиливается боль в груди, в поздних стадиях развивается легочно-сердечная недостаточность. Решающими критериями диагностики служат данные профессионального анамнеза в сочетании с типичными рентгенологическими признаками силикоза. Лечебные мероприятия включают бронхоальвеолярный лаваж, медикаментозную терапию, оксигенотерапию; в отдельных случаях – трансплантацию легких.
МКБ-10
Общие сведения
Причины силикоза
Скорость развития заболевания, распространенность и тяжесть поражения зависит от стажа работы, условий труда, интенсивности пылевого воздействия, индивидуальных свойств организма. От начала работы на вредном производстве до выявления силикоза может пройти от 3-5 до 15-20 лет. Существенное значение имеет размер пылевых частиц – для проникновения в альвеолы и межуточную ткань диаметр пылинок должен составлять менее 5 мкм. Обсуждается несколько теорий патогенеза силикоза. Наиболее ранняя из них – механическая объясняет патологические изменения механическим повреждением легочной ткани мелкодисперстной пылью. Согласно токсико-химической теории, кварцевая пыль растворяется в тканях с выделением кремниевой кислоты, оказывающей цитотоксическое действие. Однако эти и другие теории не могут до конца объяснить всех аспектов патогенеза.
Классификация
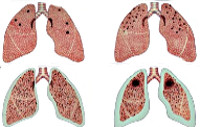
Различают три основные клинико-морфологические формы силикоза – узелковую, диффузно-склеротическую и смешанную. При узелковой форме силикоза в легких формируются силикотические гранулемы, представленные пучками соединительной ткани. Гранулемы могут располагаться концентрически или вихреобразно, иногда сливаются в крупный узел (узловая или опухолевидная форма силикоза). Узелки могут подвергаться некротическим изменениям и при прорыве в бронх образовывать силикотические каверны. Диффузно-склеротическая форма протекает с развитием межальвеолярного, периваскулярного и перибронхиального фиброза; формированием бронхоэктазов, эмфиземы, плевральных шварт. При смешанной форме силикоза на фоне распространенного склероза выявляются узелковые гранулемы.
Силикоз может протекать в острой, хронической (классической), прогрессирующей, ускоренной форме. Острый силикоз развивается при массивном воздействии кремниевой пыли в сроки менее 2-х лет. Протекает бурно с сильнейшей одышкой, общими симптомами (слабостью, потерей веса). Хронический силикоз обычно дает о себе знать через 15 и более лет после контакта с кремнеземом. Развивается асимптомно, исподволь, а усиление одышки и кашля часто списывается на другие заболевания или естественный процесс старения. Протекает в форме узелкового фиброза.
Для прогрессирующего массивного фиброза характерна усиленная одышка, кашель с мокротой, рецидивирующие гнойные бронхиты, выраженные нарушения легочной вентиляции. Типичными осложнениями данной формы силикоза служат пневмоторакс, туберкулез, легочное сердце. Ускоренный вариант силикоза возникает через 5-10 лет контакта с кварцевой пылью. Клинические проявления схожи с хронической формой, однако прогрессируют быстрее. Часто сочетается с микобактериальной инфекцией, аутоиммунными заболеваниями (склеродермией).
Симптомы силикоза
В большинстве случаев заболевание развивается постепенно, при этом субъективные клинические симптомы силикоза появляются позднее рентгенологических изменений в легких. На основании клинико-рентгенологических признаков выделяют три стадии силикоза.
На I стадии одышка присутствует только в условиях физического напряжения, больного беспокоит периодический сухой кашель, умеренные покалывающие боли в груди. Рентгенологически определяется усиление легочного рисунка, начальные признаки эмфиземы.
II стадия силикоза сопровождается одышкой при минимальной нагрузке, надсадным кашлем, постоянными болями в грудной клетке. Выслушиваются сухие рассеянные хрипы, жесткое дыхание. На снимках выявляются узелковые элементы, плевральные наслоения, буллезная эмфизема.
На последней, III стадии силикоза одышка становится постоянной (в т. ч. в покое), беспокоит кашель с мокротой, кровохарканье, тахикардия; выявляется цианоз лица. В поздних стадиях развивается легочная гипертензия и сердечно-легочная недостаточность. Рентгенологические признаки включают массивный пневмофиброз, эмфизему, ателектазы, смещение средостения.
Диагностика
Достоверность диагноза «силикоз» подтверждается после уточнения профессионального маршрута, проведения рентгендиагностики, исследования ФВД, консультаций пациента профпатологом и пульмонологом. Аускультативные данные пестрые: над разными участками легкого может выслушиваться жесткое, ослабленное, бронхиальное дыхание, сухие трескучие и влажные хрипы, шум трения плевры.
Основными рентгенологическими признаками силикоза служат силикотические узелки – мелкоочаговые тени округлой формы размером от 1 до 10 мм, расположенные в верхних легочных полях; дополнительными – эмфизема, сетчатая или ячеистая структура легочного рисунка, утолщение плевры. КТ легких высокого разрешения или МСКТ обладают более высокой чувствительностью. Данные спирографии выявляют смешанные нарушения легочной вентиляции (снижение ЖЁЛ, ОФВ1, пробы Тиффно и др.). Контролировать динамику развития силикоза позволяет исследование газов крови, пульсоксиметрия. У некоторых пациентов выявляются антиядерные антитела, С-реактивный белок, положительный ревматоидный фактор.
Дифдиагностику силикоза следует осуществлять с саркоидозом, гемосидерозом, антракозом, асбестозом, милиарным туберкулезом, метастатическим раком легкого, гранулематозом Вегенера, грибковыми поражениями легких. Отличить силикоз от перечисленных заболеваний помогает дополнительный комплекс исследований (анализ мокроты, бронхоскопия, туберкулиновая проба, ПЭТ и КТ грудной клетки).
Лечение силикоза
Радикальные методы лечения силикоза не разработаны. При подтверждении диагноза первоочередной мерой должно стать прекращение контакта с кварцевой пылью. Назначается белковое и витаминизированное питание, лечебная гимнастика, ходьба на расстояние. Основной целью терапии является торможение прогрессирования фиброзных изменений, предупреждение и устранение осложнений.
В части случаев лечение начинают с тотального бронхоальвеолярного лаважа – эта методика помогает снизить общее пылевое загрязнение легких. При быстром прогрессировании силикоза используются кортикостероидные гормоны (преднизолон). Положительный эффект отмечается от ингаляций протеолитических ферментов, улучшающих бронхиальную проходимость, и гиалуронидазы, увеличивающей проницаемость тканей для используемых медикаментов.
В комплексную терапию силикоза включаются бронхолитики (беротек, сальбутамол), отхаркивающие, антигистаминные средства, оксигенотерапия. В случае присоединения туберкулезного процесса показано лечение у фтизиатра. Меры физиотерапевтической реабилитации включают ультразвук, УФО, электрофорез, дыхательную гимнастику, санаторно-курортное лечение. Больным силикозом необходим категорический отказ от курения, профилактическая вакцинация против гриппа, пневмококка. При тяжелом, быстро прогрессирующем легочном фиброзе единственным спасением может служить трансплантация легких.
Прогноз и профилактика
Своевременно распознанный, неосложненный силикоз может не оказывать существенного влияния на качество и продолжительность жизни. Однако во всех случаях изменения в легких необратимы, а заболевание будет прогрессировать с той или иной скоростью. Неблагоприятные исходы регистрируются при быстро прогрессирующих и осложненных формах пневмокониоза.
Основу профилактических мероприятий составляет улучшение санитарно-технических условий (герметизация оборудования, автоматизация производственных процессов, вытяжная вентиляция, использование индивидуальных средств защиты и т. п.). Предупредительные меры медицинского характера включают периодические профосмотры с обязательным рентгенологическим исследованием легких. Лица, больные силикозом, освобождаются от работы на вредных производствах, в зависимости от тяжести расстройств им присваивается группа инвалидности.
Расширение возможностей повышения эффективности и безопасности лечения силикоза
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Необратимость течения силикоза и отсутствие патогенетических методов лечения делают особенно актуальной задачу поиска новых методов фармакотерапии.
Приводится теоретическое и практическое обоснование целесообразности изучения возможности использования для лечения и профилактики силикоза лимфотропного лекарственного средства – Лимфомиозот, препарата нормализующего функциональные процессы в слизистой бронхов – Мукоза композитум и универсального антитравматического лекарства – Траумель С.
Цель: изучение лечебного эффекта лекарственных средств при силикозе и изучение их протективного действия в группе лиц, которым был поставлен диагноз «подозрение на силикоз».
Материал и методы: диагноз «силикоз» выставлялся с учетом данных санитарно-гигиенических условий труда, клинического, рентгенологического и функционального исследования в соответствии с классификацией пневмокониозов. Проведенное клиническое исследование является проспективным рандомизированным плацебо-контролируемым.
Результаты и обсуждение: об эффективности фармакотерапии у больных силикозом свидетельствует положительная динамика изменений субъективных и объективных клинических признаков, показателей функции внешнего дыхания, бронхофиброскопии и гистограмм биоптатов слизистой оболочки бронхов. Протективный эффект подтвержден в группах лиц с подозрением на силикоз. Назначение препаратов снижало вероятность развития неблагоприятного исхода. Неблагоприятным исходом считалась постановка диагноза в группах лиц с подозрением на силикоз, получавших и не получавших антигомотоксические лекарственные средства в течение 2-х лет. Предложены соответствующие схемы лечения и профилактики. Схема лечения: Мукоза композитум 2 раза в неделю с интервалом в 3 дня внутримышечно по 2,2 мл. В промежутках между днями инъекций чередовать через день 3-разовый прием по 10 капель препаратов Лимфомиозот и Траумель в 1/4 стакана воды. Схема профилактической фармакотерапии: введение Мукоза композитум 2 раза в неделю с интервалом в 3 дня внутримышечно по 2,2 мл (10 ампул) 2 раза в год пациентам с подозрением на силикоз (силикоз 0-1).
Ключевые слова: силикоз, проспективное рандомизированное плацебо-контролируемое клиническое исследование, Лимфомиозот, Мукоза композитум, Траумель С.
Для цитирования: Шпигель А.С., Вакурова Н.В. Расширение возможностей повышения эффективности и безопасности лечения силикоза // РМЖ. 2016. № 16. С. 1065–1072.
Для цитирования: Шпигель А.С., Вакурова Н.В. Расширение возможностей повышения эффективности и безопасности лечения силикоза. РМЖ. 2016;16:1065-1072.
Expanding possibilities to improve efficacy and safety of silicosis treatment
Shpiegel A.S., Vakurova N.V.
Samara State Medical University
Key words: silicosis, prospective, randomized, placebo controlled clinical trial, Limfomiozot, Mucosa compositum, Traumeel S.
For citation: Shpiegel A.S., Vakurova N.V. Expanding possibilities to improve efficacy and safety of silicosis treatment // RMJ. 2016. № 16. P. 1065–1072.
Статья посвящена вопросам лечения силикоза
Введение
Необратимость течения силикоза и отсутствие патогенетических методов лечения делают особенно актуальной задачу поиска новых методов фармакотерапии [1–3].
Наше внимание к оценке возможности использования современных гомеопатических препаратов для лечения и профилактики силикоза обусловлено общеизвестным обстоятельством, согласно которому патологические синдромы и симптомы, наблюдаемые в клинике профессиональных болезней, служат поводом для разработки гомеопатических лекарственных средств.
Возникновение силикоза, с одной стороны, подтверждает правомерность гомеопатического постулата, согласно которому инертное вещество при растирании, измельчении может стать биологически активным, с другой – технология приготовления гомеопатических препаратов путем последовательного их потенцирования или динамизации в определенной мере имеет сходство с активированием кварцевой пыли в организме. Без последовательной смены процесса фагоцитоза, гибели и распада кониофагов пыль, даже кварцевая, не обладает прямым фиброгенным эффектом [4].
Теоретические предпосылки возможности использования препаратов Лимфомиозот, Мукоза композитум и Траумель С для лечения и профилактики силикоза
Очищение легких от пыли происходит преимущественно бронхогенным путем, меньшее количество пылевых частиц выводится через лимфатические пути в трахеобронхиальные узлы [1].
Однако чрезмерная пылевая нагрузка приводит к активации лимфогенного пути выведения пыли, перегрузка лимфогенного пути – к инфильтрации кониофагами (макрофагами, поглотившими пыль) зоны корней лимфатических сосудов, затем и более крупных сосудов. Развивается кониотический лимфангит, который способствует формированию кониотических гранулем [4, 5].
Внедрение и широкое использование бронхофиброскопии с биопсией и гистологическим изучением биоптатов, исследование бронхоальвеолярного секрета, иммунологические, цитологические, цитохимические и другие методы исследования позволили получить дополнительные данные о сущности патологических процессов в органах дыхания, механизмах формирования и течения заболеваний, возникающих от воздействия промышленных аэрозолей различного состава [5–7].
Под пневмокониозом следует понимать профессиональные заболевания легких от воздействия промышленной пыли, проявляющиеся хроническим диффузным пневмонитом с развитием фиброза легких.
Пневмокониоз, как диффузный пневмонит, морфологически проявляет себя в 2-х главных формах: интерстициальной и интерстициально-гранулематозной. При обеих формах тканевые нарушения в легких складываются до определенного момента из однотипных морфологических изменений, хотя длительность и степень их выраженности могут варьировать в зависимости от характера и вида пыли.
Длительное присутствие пыли в организме приводит к вовлечению в патологический процесс все новых и новых участков легких, в связи с чем у одного и того же больного кониотический процесс находится в различных сегментах легкого на разных стадиях морфологического развития.
Патоморфологически в развитии любой формы и вида пневмокониоза предложено выделить 2 периода: 1-й – воспалительно-дистрофических нарушений; 2-й – продуктивно-склеротических изменений.
Первый период длится до тех пор, пока преобладают тканевые нарушения первых 3-х стадий морфогенеза пневмокониоза: альвеолярного липопротеиноза, серозно-десквамативного альвеолита и кониотического лимфангита. Первый период воспалительно-дистрофических нарушений завершается стадией кониотического лимфангита. В этот период формируются предпосылки следующего за ним периода – продуктивно-склеротических изменений. Практически этот 2-й период совпадает с IV стадией морфогенеза пневмокониоза – стадией кониотического пневмофиброза. Главной чертой этого периода является прогрессирующее развитие пневмофиброза во всех структурах ацинусов и долек легкого. При этом в основе бурного развития соединительной ткани лежит несколько причин. Основной из них является нарушение лимфодинамики органа. Выведение пылевых частиц лимфогенно, через лимфатические коллекторы ацинуса, в условиях продолжающегося воздействия пыли является центральным звеном в формировании кониотического процесса в легких [4–6]. Полагают, что в патологический процесс на первых его этапах включаются лимфатические капилляры вокруг посткапиллярных венул кровеносных сосудов малого круга кровообращения. Более крупные лимфатические коллекторы и кровеносные сосуды вовлекаются в процесс позднее.
В респираторных отделах легких развивается серозно-десквамативный альвеолит, которому предшествует альвеолярный липопротеиноз. Указанный альвеолит завершается десквамативной инфильтративной обтурацией альвеол и бронхиол, что приводит к формированию кониотического лимфангита.
При этом в слизистой оболочке бронхов разворачиваются компенсаторно-приспособительные процессы, которые можно обозначить как хронический эндобронхит, прогрессирующий от катарального до катарально-склерозирующего и склерозирующего вида эндобронхита [4–6].
Вышеописанные положения явились теоретическим обоснованием целесообразности изучения возможности использования для лечения и профилактики силикоза лимфотропного лекарственного средства Лимфомиозот, препарата нормализующего функциональные процессы в слизистой бронхов – Мукоза композитум и универсального антитравматического лекарства – Траумель С.
Цель: изучить лечебный эффект гомеопатических лекарственных средств при силикозе и их протективное действие в группе лиц, которым был поставлен диагноз «подозрение на силикоз».
Материал и методы исследования
Для подтверждения или исключения диагноза проводилось рентгенологическое исследование в соответствии с требованиями, предъявляемыми к этой процедуре. Функциональные исследования органов дыхания и бронхофиброскопические исследования проводили с помощью компьютерного пневмотахографа «Custo Vit» (Германия). Исследуемые величины выражались в процентах к должным.
Радиоизотопные исследования выполнены на кафедре лучевой диагностики СамГМУ.
Для оценки регионарной вентиляции легких на фоне гомеопатической фармакотерапии у 14 человек применялась ингаляционная аэрозольная сцинтиграфия легких, которая выполнялась c помощью установки «Venticis II» (CIS International, Франция). Информативность данного метода в выявлении регионарных нарушений вентиляции превосходит возможности функциональных тестов и обладает некоторыми преимуществами перед исследованиями с применением радионуклидов инертных газов [12].
Бронхофиброскопия проводилась под местной анестезией 10% раствором лидокаина на аппарате «Olympus BF» тип P10 c записью на видеоблоке OTB/F-3 с последующей биопсией слизистой оболочки со шпор сегментарных бронхов бронхиального дерева и гистологическим исследованием биоптатов.
Фиксация биопсийного материала осуществлялась в 10% растворе формалина с последующей заливкой в парафиновые блоки. Срезы толщиной до 10 мкм окрашивались гематоксилин-эозином. Микропрепараты консультированы на кафедре патологической анатомии СамГМУ. При бронхофиброскопическом исследовании и гистологическом изучении биоптатов слизистой оболочки бронхов до лечения были выявлены общеизвестные признаки длительного воздействия производственной пыли [2, 6].
Для изучения возможности расширения показаний к антигомотоксической фармакотерапии была разработана собственная программа клинических испытаний. Согласно принципам клинической фармакологии настоящая работа может быть отнесена к клиническим испытаниям IV фазы, суть которых заключается в расширении показаний к применению комплексных антигомотоксических лекарств у больных силикозом. Проведенное клиническое исследование является проспективным рандомизированным простым слепым плацебо-контролируемым. В качестве контрольных лекарственных средств использовали плацебо или общепринятое лечение силикоза. Так как ни одно из известных лекарственных средств не имеет высокой эффективности при силикозе и на первых этапах заболевание даже без лечения протекает относительно доброкачественно, для оценки эффективности антигомотоксического лечения сравнение проводили с группой больных, получавших плацебо. По внешнему виду плацебо и исследуемое лекарственное средство были идентичными. Для реализации слепого метода контроля специального изготовления веществ не требовалось. Физиологический раствор при парентеральном введении и водно-спиртовой раствор соответствующей концентрации по внешнему виду, консистенции, вкусу были идентичны исследуемым лекарственным средствам.
Процедура рандомизации была разработана до начала клинических испытаний. Случайное распределение вида лечения определено методом случайных чисел на компьютере. Перед проведением рандомизации обследуемые и больные были стратифицированы по параметрам, включая профмаршрут (работа на одном предприятии – горно-обогатительном комбинате), санитарно-гигиенические условия труда.
Наблюдения проводились в заранее определенные протоколом промежутки времени: до начала лечения, в ходе лечения, по завершении лечения. Оценку эффективности проводили после окончания первоначального и 2-х последующих курсов в стационаре (через 1 и 2 года). Больные в течение года, предшествующего исследованиям, не лечились от данного заболевания.
Результаты вмешательства оценивались в соответствии с принципами доказательной медицины [9–11]. Эффективность лечения определялась числом исследуемых, у которых произошло улучшение клинико-функциональных характеристик. Использовали систему количественных шкал – определенный набор изменений клинической картины заболевания по сравнению с исходным уровнем. Высокая оценка в баллах могла быть дана в зависимости от количества субъективных и объективных признаков заболевания. Таким образом, чем меньше степень исчезновения этих признаков, тем выше оценка в баллах. Оценки представляли собой произвольно выбранные числа, которые несли только информацию, показывающую, что при оценке «6 баллов» состояние больного лучше, чем при оценке «3 балла», но не свидетельствовали, что состояние первого больного в 2 раза лучше, чем второго.
Результаты и обсуждение
Диагноз «силикоз» выставлялся с учетом санитарно-гигиенических условий труда, данных клинического, рентгенологического и функционального исследования в соответствии с классификацией пневмокониозов.
Содержание кремнийсодержащей (кварцевой) пыли в воздухе производственных помещений в отдельные моменты технологического процесса значительно превышало предельно допустимые концентрации, содержание свободной двуокиси кремния достигало 98,2%, с размерами пылевых частиц менее 2 мкм – 26%, 2–5 мкм – 65%. Высокая степень дисперсности обеспечивает длительное пребывание пыли в воздухе производственных помещений и глубокое проникновение в органы дыхания работающих. Условия труда были отнесены к III степени вредности с повышенной опасностью развития профессиональных заболеваний по пылевому фактору. Относительные показатели профессиональной заболеваемости на изучаемом производстве превышали областной показатель и были значительно выше в целом по отрасли.
Влияние изучаемой фармакотерапии на изменение субъективных и объективных клинических признаков
Основное препятствие при оценке эффективности лечения и профилактики силикоза изучаемыми препаратами – это скудность клинической симптоматики силикоза и малая эффективность применяемой симптоматической терапии [2, 3, 8]. В связи с этим оценка состояния больного (с точки зрения исчезновения симптомов заболевания) по конечным показателям для сравнения эффективности изучаемых и контрольных лекарственных средств была затруднена. Поэтому рассчитывать на высокую демонстративность исчезновения субъективных и объективных признаков заболевания не представлялось возможным. Сроки разрешения объективных и субъективных признаков заболевания лишь в известной мере могли служить критерием относительной эффективности испытываемой и обычной терапии.
Эффективность гомеопатического лечения силикоза оценена в динамике в течение 2-х лет у 89 человек: 29 получавших антигомотоксическое лечение; 30 – плацебо; 30 – обычную общепринятую фармакотерапию.
По возрасту и стажу работы группа контактных пациентов и группа больных не имела достоверных отличий (р>0,05). Мужчины составляли 78%, женщины – 22%. Лица со стажем работы более 10 лет составили 80%.
Пациенты 1-й группы получали лечение изучаемым методом в течение 21 дня пребывания в профцентре по схеме: Мукоза композитум внутримышечно по 2,2 мл 2 раза в неделю с интервалом в 3 дня. В промежутках между днями инъекций через день чередовали 3-разовый прием по 10 капель препаратов Лимфомиозот и Траумель С в 1/4 стакана воды. Вторая группа получала плацебо, третья – обычное, общепринятое в областном профцентре лечение.
Во 2-й и 3-й группах в процессе лечения субъективные и объективные изменения оказались относительно одинаковы. По-видимому, это связано не только с неэффективностью общепринятого лечения силикоза, но и с тем, что его проведение в настоящее время минимально или вообще не проводится. В связи с вышеизложенным мы сочли возможным и корректным приводить результаты оценки эффективности изучаемого метода в основном по сравнению с группой больных, получавших плацебо.
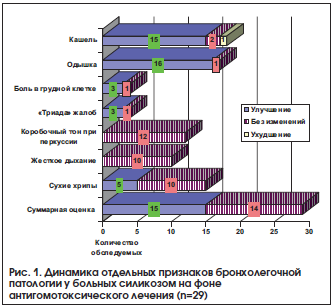
На рисунках 1 и 2 соответственно представлены изменения субъективных и объективных признаков силикоза в динамике лечения в стационаре изучаемым методом (1-я группа) и методом плацебо (2-я группа). Из рисунков видно, что после 1-го курса лечения в стационаре в 1-й группе самочувствие и состояние больных изменилось в большей мере, чем во 2-й и 3-й группах.
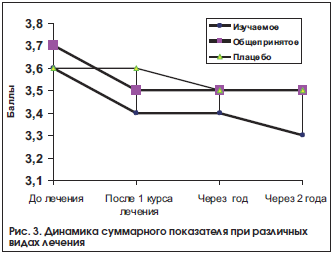
Особенно четко это прослеживается при сравнении суммарной оценки эффективности результатов лечения. На рисунке 3 приведены результаты контроля эффективности лечения на основе использования суммарной оценки субъективных и объективных признаков патологии бронхолегочной системы.
Суммарная оценка складывалась из 7 отдельных оценок от 0 (симптом отсутствует) до 1 – симптом имеется. Максимально достижимая суммарная оценка составляла 7 баллов. Результаты оценивались в динамике до и после 1-го курса лечения в стационаре, через 1 и 2 года (повторное наблюдение и лечение в стационаре).
Как видно из представленных данных, суммарная оценка при проведении гомеопатической фармакотерапии значительно снизилась после курса лечения и имела тенденцию к снижению после повторных курсов лечения. Общепринятое лечение и плацебо-лечение тоже приводило к снижению данного показателя, но в меньшей степени, и не отмечалось тенденции к его уменьшению при проведении повторных курсов обычной фармакотерапии.
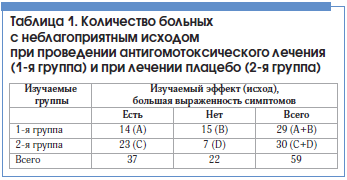
Используя суммарную оценку, мы составили таблицу сопряженности, где приведены возможные исходы эффективности лечебного воздействия (табл. 1).
В конкретном количественном выражении динамика суммарной оценки на фоне лечения в 1-й группе выглядела следующим образом: у 15 больных отмечалось улучшение, у 14 – изменений не отмечено. Во 2-й группе на фоне плацебо улучшение отмечено только у 7, у 21 изменений не выявлено, у 2-х больных наблюдалось ухудшение. То есть у 23 пациентов отмечено отсутствие эффекта в лечении, наличие неблагоприятного исхода, большая выраженность симптомов.
Согласно этим данным рассчитаны ключевые показатели эффективности лечения в 1-й группе пациентов, получавших антигомотоксическую фармакотерапию, в сравнении со 2-й группой пациентов, получавших плацебо (табл. 2).
Результаты, приведенные в таблице 2, характеризуют довольно высокую частоту неблагоприятных исходов в группе контроля – 77% (у пациентов, получавших плацебо) по сравнению с группой больных, принимавших антигомотоксические лекарственные средства – 48% (p Литература