Что такое диабетическая стопа? Причины возникновения, диагностику и методы лечения разберем в статье доктора Есипенко И. А., сосудистого хирурга со стажем в 36 лет.
Определение болезни. Причины заболевания
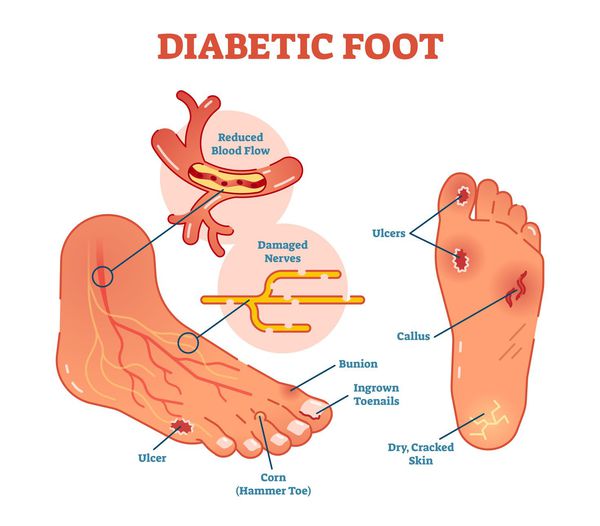
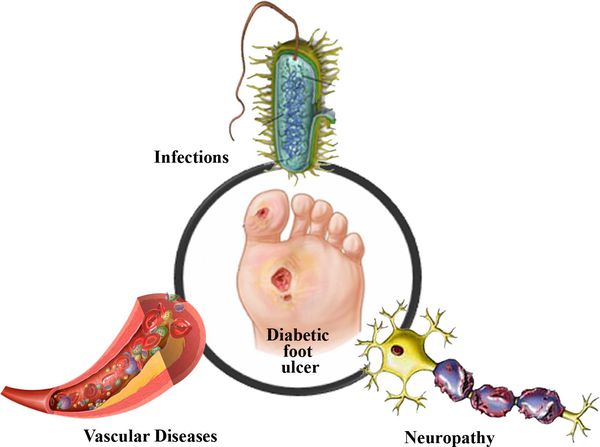
Диабетическая стопа (синдром диабетической стопы, СДС) — это тяжёлое осложнение сахарного диабета в виде инфекции, язв или разрушения глубоких тканей, которое возникает в связи с нарушением макроструктуры стопы и микроциркуляции крови, по причине разрушения нервных окончаний и нервных волокон. [1]
Главная причина ДС — это Сахарный диабет (СД). И хотя синдром диабетической стопы не развивается с первого дня увеличения уровня глюкозы в крови более 7,0-8,0 ммоль/л, каждый пациент с диагнозом «Сахарный диабет» должен помнить о таком грозном возможном осложнении.
СДС развивается в разной степени и разных формах:
Основные «пусковые механизмы» развития язв при СДС:
1. Ношение неудобной обуви. К изменению нагрузки на суставы стопы, сдавливанию или потёртости кожи, локальной микроишемии, инфильтрату, или некрозу могу привести любые дефекты обуви:
2. Увеличенный вес тела. Учитывая площадь стоп, при увеличении веса тела (даже на 1 кг) увеличивается и нагрузка на каждый сустав стопы. Самая уязвимая область — подошвенная поверхность.
3. Разрастание эпидермиса (поверхности) кожи. Этот процесс происходит из-за нарушенных обменных процессов в коже на фоне СД (под утолщённым эпидермисом-«мозолью» в слоях кожи нарушается микроциркуляция, что приводит к микроишемии и некрозу).
4. Микротравмы:
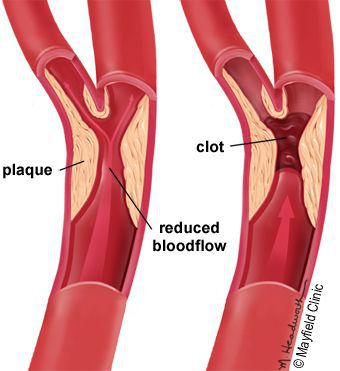
5. Стенозы (сужение) и окклюзии (закупорка) магистральных артерий. В результате отсутствия кровоснабжения в стопах и голенях к микроишемии присоединяется макроишемия и развитие гангрены конечности.
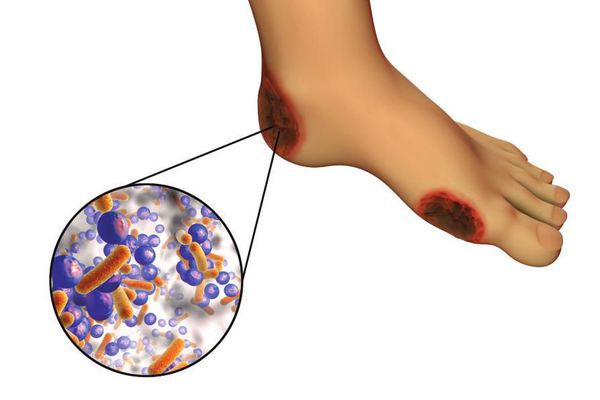
6. Условно патогенная или патогенная микрофлора. Активизация флоры (микробов и других микроорганизмов) на поверхности кожи в условиях СД приводит к воспалению кожного покрова, а в условия ишемии или микротравмы значительно ускоряется развитие гангрены.
Часто наблюдается сочетание нескольких причин возникновения язв при СДС.
Симптомы диабетической стопы
Отправной точкой развития СДС считается не дата установления диагноза «Сахарный диабет», а время, когда были выявлены первые симптомы СД (однократные подъёмы глюкозы крови, сухость во рту и другие).
Симптомы СДС:
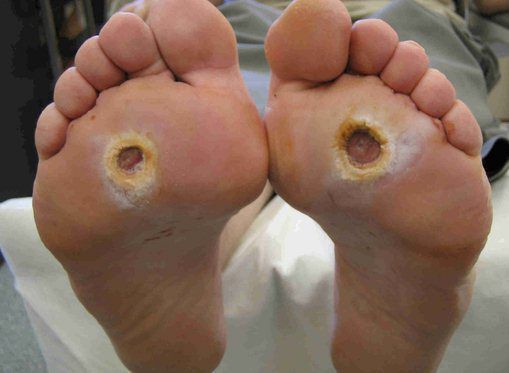
Чаще всего трофическим изменениям подвержены дистальные отделы конечности: пальцы и подошвенная поверхность стопы в проекции головок плюсневых костей. Зона образования трофической язвы зависит от причины её возникновения.
Патогенез диабетической стопы
Механизм развития СДС представляет собой следующую патологическую последовательность:
Таки образом, при СДС происходит повреждение всех тканей нижней конечности.
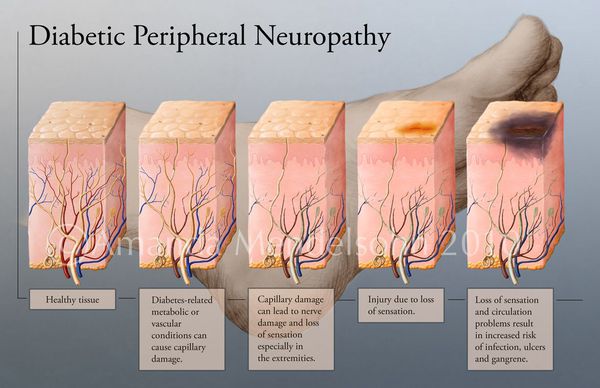
В результате дефицита инсулина в организме диабетика количество глюкозы в крови увеличивается. Это в свою очередь негативно сказывается на состоянии как мелких, так и крупных сосудов:
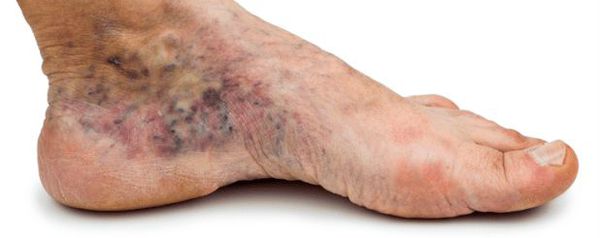
В результате этих изменений кровообращение нарушается и образуются небольшие тромбы. Эти изменения в организме препятствуют поступлению достаточного количества микроэлементов и кислорода в клетки и тем самым приводят к нарушениям обменного процесса. Кислородное голодание тканей замедляет процесс деления клеток и провоцирует их распад.
Увеличение уровня глюкозы в крови также становятся причиной поражения нервных волокон — снижается чувствительность.
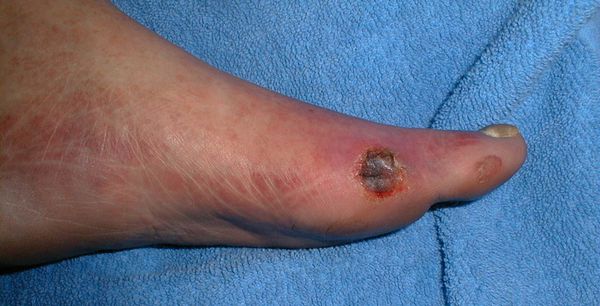
Все деструктивные процессы, происходящие в тканях стопы приводят к тому, что любое повреждение кожи становится лёгким процессом, а заживление — длительным. Усугубить состояние стопы могут присоединившиеся инфекции, которые способны привести к образованию гангрены — некрозу тканей. [9]
Классификация и стадии развития диабетической стопы
Классификация I Международного симпозиума по диабетической стопе
В 1991 году в Нидерландах на I Международном симпозиуме была принята классификация СДС, которая является наиболее распространённой. [1] Она предполагает разделение заболевания на три типа в зависимости от преобладающего патологического процесса:
Классификация Вагнера
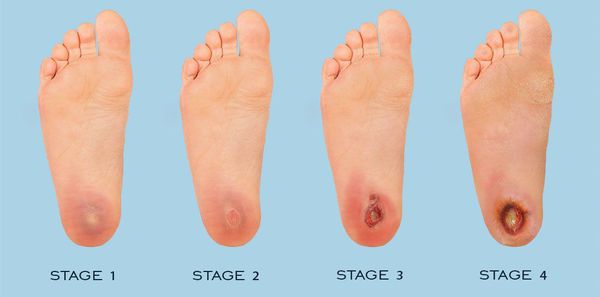
По степени выраженности поражений тканей стопы выделяют следующие стадии СДС: [6] [7]
Классификация Техасского университета
Данная классификация была разработана в 1996-1998 годах. [8] В её основе лежит оценка язвы по глубине, наличию инфицирования и ишемии — риска ампутации конечности.
Урок 11. Осложнения на ноги
Причины поражения стоп
У пациентов с сахарным диабетом достаточно часто возникают различные патологические изменения стоп, причем даже обычные проблемы (например, мозоли или трещины) могут привести к серьезному осложнению — синдрому диабетической стопы (язва на стопе, гангрена стопы).
Основными причинами развития поражений стоп при сахарном диабете являются:
Периферическая нейропатия
С одной стороны, симптомами периферической нейропатии могут быть боль, ощущение ползания мурашек, судороги, с другой — пораженные нервные волокна теряют чувствительность к боли, теплу и холоду, давлению. Это значит, что вы можете не почувствовать травму: например, вы можете не заметить инородный предмет в ботинке или ожог при согревании ног около камина или батареи до тех пор, пока уже не образуется рана.
Деформация пальцев и свода стопы
Поражение нервных волокон может привести к деформации пальцев и свода стопы, что, в свою очередь, также может закончиться язвенными дефектами стоп. Если у вас есть какие-либо изменения: «косточки», плоскостопие, деформация пальцев — спросите своего врача, где можно заказать или приобрести ортопедическую обувь. Ношение индивидуальной ортопедической обуви — обязательная профилактика возникновения язв стопы.
Снижение кровотока в артериях нижних конечностей (атеросклероз артерий нижних конечностей)
Основными причинами развития атеросклероза при сахарном диабете являются:
Таким образом, для профилактики развития атеросклероза надо контролировать все эти факторы. Основным клиническим симптомом атеросклероза артерий нижних конечностей является возникновение боли при ходьбе — так называемая перемежающаяся хромота, которая проходит через некоторое время после остановки. Если у вас есть этот симптом, вы незамедлительно должны бросить курить. Также необходимо регулярно принимать препараты, контролирующие артериальное давление и снижающие уровень атерогенных липидов в крови. В некоторых случаях могут быть эффективны препараты, улучшающие периферический кровоток.
При плохом кровообращении ваши ноги могут постоянно мерзнуть. Помните, что нельзя согревать ноги на батарее, у открытого огня, парить в горячей воде — это может привести к образованию ожогов и язвенных дефектов, поскольку у вас также может быть нейропатия, т.е. вы не будете чувствовать высокую температуру. Лучший способ согреть ноги — носить теплые носки.
Как возникают проблемы с ногами?
Повреждения кожи
Кожа при сахарном диабете становится очень сухой, что может привести к ее шелушению и появлению трещин. Все дело в том, что поражаются нервные волокна, отвечающие за водный и липидный баланс кожи. Повреждения заживают длительно, а кроме того, могут инфицироваться. Вероятность этого особенно велика при высоком уровне глюкозы в крови. Для профилактики трещин и шелушения после ванны ноги тщательно вытирают, уделяя особое внимание межпальцевым промежуткам. Для предотвращения появления трещин необходимо мазать подошвы и пятки увлажняющим кремом, при этом нельзя втирать крем в межпальцевые промежутки.
Мозоли и натоптыши
При сахарном диабете мозоли встречаются гораздо чаще и нарастают гораздо быстрее, чем у остальных людей. Это обусловлено деформацией пальцев и свода стопы, а также перераспределением зон высокого давления. Таким образом, мозоли могут являться свидетельством того, что вам необходимы ортопедические корректоры или обувь.
Если своевременно не удалять мозоли, то они будут трескаться и инфицироваться, приводя к развитию язвенных дефектов. Однако самим удалять большие и старые мозоли опасно. Лучше обратиться в кабинет «Диабетической стопы», где опытный персонал при помощи специального аппарата обработает вам ноги.
Ежедневная обработка натоптышей и мозолей с помощью пемзы поможет предотвратить их нарастание, причем лучше всего использовать пемзу после душа или ванны, пока кожа еще влажная. Ни в коем случае нельзя пользоваться бритвенными лезвиями или терками, а также какими-либо химическими растворами — это может привести к повреждению или ожогам и дальнейшему инфицированию. После обработки мозолей пемзой необходимо смазывать их кремом.
Синдром диабетической стопы
Иногда пациенты говорят: «У меня диабетическая стопа», подразумевая, что так называется нога при сахарном диабете. На самом деле синдром диабетической стопы — это очень серьезное осложнение сахарного диабета, проявляющееся наличием язвы на стопе.
Язвенные дефекты чаще всего образуются в местах наибольшего давления: головки плюсневых костей, межфаланговые сочленения при деформации пальцев. Язвенные дефекты на боковых поверхностях стоп чаще всего свидетельствуют о тесной обуви.
Даже если язва никак вас не беспокоит, вы немедленно должны проконсультироваться с вашим лечащим врачом или врачом кабинета «Диабетическая стопа».
В зависимости от состояния вашей язвы, врач:
После заживления язвенного дефекта вы должны соблюдать правила ухода за ногами и при необходимости носить ортопедическую обувь.
Подробнее о правилах ухода за ногами при СД
Что человек с диабетом может увидеть при осмотре стоп?
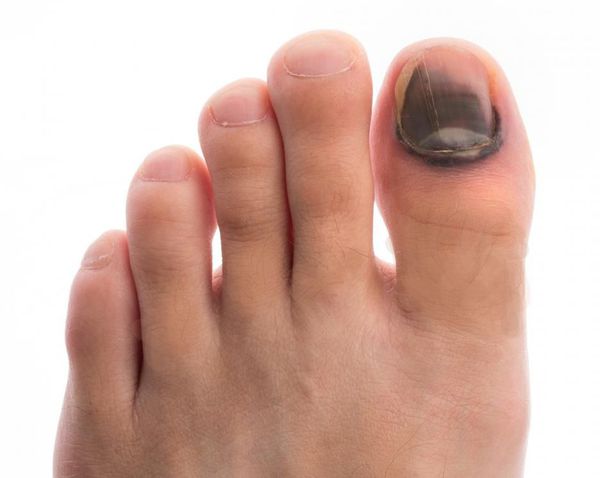
Потемнение ногтя
Эта проблема чаще всего вызывает необоснованные страхи Причина. В подавляющем большинстве случаев это – подногтевое кровоизлияние (гематома). Его развитию способствует ломкость сосудов, но основная причина – хроническое давление ногтевой пластинки на кожу пальца (ногтевое ложе). Такое возможно, если пациент сознательно носит (разнашивает) тесную обувь, но чаще – если из-за сниженной чувствительности пациент не замечает, что обувь чуть тесновата, или что ноготь слишком длинный или слишком толстый, и не помещается в обычной обуви. Чем это опасно? Если не прекращается давление ногтя на палец, кровоизлияние может увеличиваться. Результатом может быть его нагноение. Если нет нагноения – само по себе кровоизлияние лечения не требует, но оно является первым сигналом о том, что палец находится в стесненных условиях, и если проигнорировать этот сигнал – то следующим событием может стать диабетическая язва этого пальца Что делать? Понять, каким образом ноготь подвергся давлению. Вспомнить, какую обувь Вы носили в последние недели. Проверить всю обувь: рукой – для исключения посторонних предметов в обуви в области пальцев, с помощью картонной стельки убедиться, что площадь обуви не меньше площади стопы. Измерить высоту обуви в области пальцев: если она меньше, чем толщина пальца – это создает избыточное давление на ноготь. Обязательно нужно прекратить ношение той тесной обуви, которая вызвала кровоизлияние.
Вросший ноготь
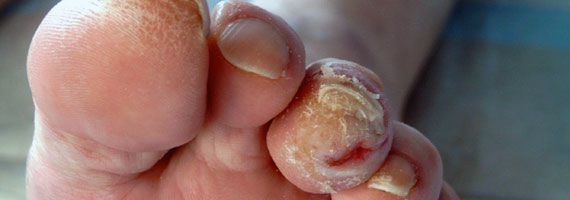
Грибковое поражение ногтя / утолщение ногтя
Причина: Грибковое поражение (микоз) проявляется изменением цвета ногтя (нарушение его прозрачности), его расслоением, в тяжелых случаях – утолщением. Микоз – наиболее частая причина утолщения ногтей, хотя возможны и другие: травма ногтя в прошлом, нарушение его питания, и т.п. Различные неприятные ощущения (зуд и т.п.) характерны для грибкового поражения кожи, но отсутствуют при изолированном поражении ногтей. Чем это опасно? Утолщенный ноготь требует дополнительного места в обуви, создает повышенное давление на палец. В результате под утолщенным ногтем происходит нагноение, результатом является диабетическая язва. Язва может также образоваться на соседнем пальце, если утолщенный ноготь травмирует его при ходьбе. Что делать? Для установления причины утолщения проводится лабораторное исследование соскоба с ногтя. Если подтверждается диагноз грибкового поражения – его можно и нужно излечить. Излечение грибкового поражения вполне реально и при сахарном диабете (хотя и с большим трудом, чем у людей без диабета), но требует: а). Лечения квалифицированным дерматологом, б). Применения противогрибковых препаратов не только местно, но и в виде таблеток, в). Ликвидации возможных резервуаров грибковой инфекции вне организма пациента – дезинфекция обуви и предметов обихода (существуют специальные стерилизационные камеры), лечение членов семьи при необходимости. Около 20 лет назад, когда еще не было безопасных противогрибковых препаратов в таблетках, закрепилось мнение о высокой частоте побочных эффектов такого лечения. Современные же противогрибковые препараты для приема внутрь хорошо переносятся пациентами, и риск побочных эффектов при их приеме минимален. Если утолщение ногтя связано не с грибковым поражением (или если противогрибковое лечение по каким-то причинам не проводится) – обязательно надо проводить регулярную механическую обработку ногтя, чтобы снизить его толщину до нормальной. Такую обработку можно выполнить самостоятельно (пилкой для ногтей, шлифуя ноготь по 10-15 минут в день в течение нескольких дней), или в тех педикюрных кабинетах, где оказываются такие услуги.
Порезы кожи при подстригании ногтей
Причина: Такое случается при СД довольно часто, и несет в себе серьезную опасность. Делов том, что диабет часто нарушает болевую чувствительность. Вы можете не почувствовать боли, если вместе с ногтем срезаете кусочек кожи. Риск таких порезов повышен у людей с ослабленным зрением и избытком веса, когда трудно дотянуться до своих ног. Чем это опасно? Очень часто на месте такого пореза формируется диабетическая язва. Что делать? Правильно подстригать ногти, не срезать их слишком коротко (оставляя около 1 мм длины). Если у Вас не получается подстригать ногти, если случались порезы – Вам нужно попросить о помощи родственников или постоянно пользоваться услугой профилактической обработки стоп в кабинете «Диабетическая стопа». Если Вы поранили кожу при обработке ногтей – обязательно обработайте эту ранку по всем правилам: промойте противомикробным раствором и наложите стерильную повязку.
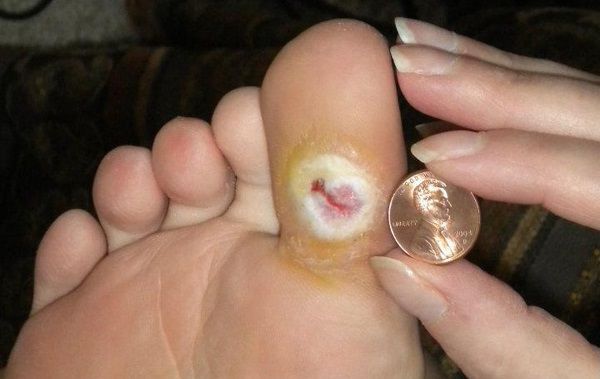
Мозоли, «натоптыши»
Мозоли встречаются не только при диабете, но при СД являются одной из частых причин образования диабетических язв. Причина. Мозоль (гиперкератоз) – защитная реакция кожи в зонах повышенного давления (механической нагрузки). Такие зоны возникают обычно из-за сочетания тех или иных деформаций стопы (плоскостопие, искривленные пальцы) и обуви, не соответствующей стопе пациента. Обычно мозоли образуются на подошвенной поверхности («натоптыши»), на верхушках пальцев, иногда – на боковой поверхности пальцев (в межпальцевом промежутке), на тыльной поверхности суставов пальцев и др. Чем это опасно? Мозоль – защитная реакция кожи, но она не совершенна. Мозоль сама является как бы инородным телом, увеличивая давление на кожу, приводя развитию кровоизлияния (темное пятно под мозолью), которое затем может нагнаиваться с образованием язвы. Что делать? Образовавшуюся мозоль нужно удалить пемзой (во время мытья), но ни в коем случае не срезать, не распаривать ноги в горячей воде, не пользоваться мозольными пластырями и жидкостями для снятия мозолей. Если давление на кожу продолжается – мозоль будет образовываться снова, и обработку пемзой придется проводить регулярно. Чтобы замедлить образование мозоли, нужно сменить обувь на более соответствующую Вашим ногам, часто – в комбинации со специальными ортопедическими стельками. Для этого надо посетить кабинет «Диабетическая стопа» или ортопеда, специализирующегося на ортопедической обуви. При межпальцевых мозолях помогает ношение межпальцевой силиконовой прокладки (продаются в аптеках и ортопедических салонах), но обувь должна быть достаточно широкой, чтобы не вызывать сдавление пальцев.
Деформации стоп
Наиболее частые деформации – выступающие «косточки» у первого пальца, клювовидные пальцы, плоскостопие и др. Причина. Обычно – заболевания суставов, мышц и связок, в очень редких случаях – переломы костей, вызванные диабетом (диабетическая остеоартропатия). Чем это опасно? Главная опасность – в том, что на выступающих участках из-за повышенного давления на кожу образуются мозоли, далее – под мозолями происходит нагноение и образование диабетической язвы. Кроме того, перегрузка тех или иных суставов из-за деформаций вызывает развитие артроза («отложения солей»), что сопровождается суставными болями. Что делать? Чтобы деформация не проводила к повышенной нагрузке на кожу, необходим подбор тех или иных ортопедических средств. Это специальная обувь и ортопедические стельки, иногда – так называемые ортопедические корректоры (например, носимые на стопе силиконовые накладки на перегруженные участки).
Обувь, не соответствующая стопе пациента
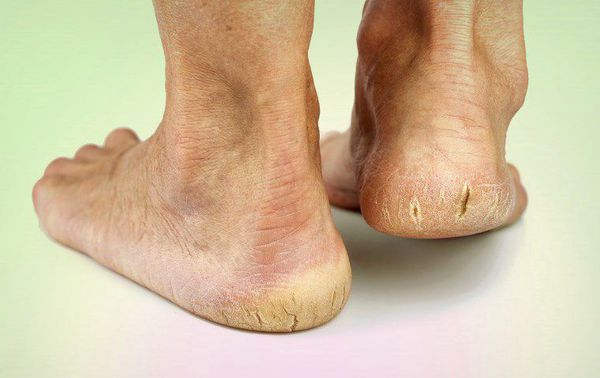
Трещины кожи пяточной области
Причина. Сухость кожи зоны пяток и повышенное ее ороговение, огрубение. Огрубение кожи усиливается при ходьбе (дома или на улице) без обуви или в обуви без задника, которая «шлепает» по пятке. Чем это опасно? Трещины кожи могут инфицироваться, превращаться в диабетические язвы. Что делать? Во-первых – полностью устранить сухость кожи на пятках, смазывая их кремом не менее 2-3 раз в день. Но крем не должен попадать между пальцами (там должно быть сухо!). Если крем не устранил сухость – надо либо смазывать чаще, либо сменить крем (на содержащий мочевину). Многие кремы пригодны для устранения сухости кожи, но наиболее эффективны те кремы и «пенки», которые содержат мочевину (Бальзамед-интенсив, Каллюзан-экстра, Алпресан №3, Диа-дерм, Heel-cream и др). Во-вторых – обрабатывать ороговевшую кожу пемзой во время мытья. В третьих, пациентам с быстрым образованием трещин нужно всегда носить обувь с задником (даже дома – есть такие виды домашних тапочек). Если имеются глубокие трещины, которые болят, кровоточат – срочно обратитесь в кабинет «Диабетическая стопа»
Грибковое поражение кожи
Когда надо срочно обратиться в кабинет «Диабетическая стопа»?
Специальная обувь для пациентов с сахарным диабетом
Она необходима примерно для 25-30% пациентов, у которых обувь, купленная в обычном магазине, не соответствует стопе (обычно это связано с теми или иными деформациями стоп). Многие пациенты с возрастом испытывают трудности при покупке обуви в обычном магазине, т.к. не могут найти обувь достаточной ширины (даже несмотря на то, что выбирают обувь большего размера, чем носили раньше). Пациентам без деформаций стоп обычно достаточно обуви, купленной в обычном магазине, но выбранной в соответствии с правилами для пациентов с сахарным диабетом (о которых говорили вначале). Ортопедическая или «полуортопедическая» (профилактическая) обувь может продаваться готовой (Lucro, Actiflex, Ortek), а для пациентов с тяжелыми деформациями ее необходимо изготавливать индивидуально (по слепку стопы). В готовую ортопедическую обувь могут быть вложены индивидуально (по слепку) изготовленные стельки. Существует серьезная проблема: далеко не вся ортопедическая обувь, которую предлагают пациентам с диабетом (платно и бесплатно) соответствует требованиям качества.
Как проверить носимую обувь?
Даже если не чувствуете тесноты, Вашу обувь надо менять, если: Вы заметили потертости, покраснение, «отпечатки» на коже Деформированные пальцы или деформации стопы «выдавливают» верх обуви При проверке картонной стелькой – площадь обуви меньше, чем площадь стопы Образуются мозоли на передней, тыльной или боковой поверхностях пальцев (проблема «натоптышей» на подошвенной может быть решена специальными стельками, однако их можно использовать лишь в просторной обуви). Если врач говорит, что Вам нужна специальная обувь. Часто требуется смена обуви, если Вам нужно изготавливать ортопедические стельки (полноценные ортопедические стельки имеют большую толщину и не входят в обычную обувь). Если врач назначил Вам ортопедическую обувь…
Особенности качественной ортопедической и «полуортопедической» обуви
Доказано, что качественная и правильная (ортопедическая) обувь в 2-3 раза снижает риск развития синдрома диабетической стопы.* Признаки правильной обуви Ширина обуви – не меньше, чем ширина стопы (особенно в области передней части стопы) Повышенная глубина (позволяющая вложить толстую ортопедическую стельку) Бесшовность и мягкость внутренней поверхности (снижает риск потертостей) Растяжимость материала верха обуви (используется мягкая кожа или искусственные материалы с более высокой растяжимостью). Отсутствие жесткой вставки в передней части обуви («подноска»), который в обычной обуви располагается перед пальцами или прикрывает их сверху. В некоторых моделях – специальная конструкция подошвы, делающая ее несгибаемой, что уменьшает нагрузку на переднюю часть стопы при ходьбе Регулируемость объема (с помощью шнурков или «липучки») на случай нарастания отека к вечеру Толщина стелек не менее 1 см, При наличии факторов риска развития синдрома диабетической стопы (деформации стопы) рекомендуется изготовление индивидуальной пары стелек, Максимальный срок службы стелек 6-12 месяцев.
Когда можно использовать ортопедические стельки в обычной обуви?
Первая помощь при повреждениях кожи стоп
Признаки правильной обуви
Минимальное количество швов («бесшовность»), Ширина обуви – не меньше, чем ширина стопы (особенно в области передней части стопы), Наличие дополнительного объема в обуви (для вложения ортопедической стельки), Отсутствие «подноска»: эластичный (растяжимый) материал верха и подкладки обуви, Регулируемость объема (с помощью шнурков или «липучки») на случай нарастания отека к вечеру, Жесткая (ригидная) подошва (обувь нельзя согнуть пополам) с перекатом, Каблук со скошенным передним краем (тупой угол между передней поверхностью каблука и основной подошвой снижает риск падений), Толщина стелек не менее 1 см, При наличии факторов риска развития синдрома диабетической стопы (деформации стопы) рекомендуется изготовление индивидуальной пары стелек, Максимальный срок службы стелек 6-12 месяцев.
Семь правил покупки и ношения правильной обуви
Лечение болевой формы диабетической полинейропатии
Диабетическая дистальная симметричная сенсорно-моторная полинейропатия (ДПН) — самый частый вариант диабетической нейропатии, который выявляется более чем у 50% больных с сахарным диабетом (СД) 1-го и 2-го типа.
Диабетическая дистальная симметричная сенсорно-моторная полинейропатия (ДПН) — самый частый вариант диабетической нейропатии, который выявляется более чем у 50% больных с сахарным диабетом (СД) 1-го и 2-го типа [1]. ДПН является второй по частоте встречаемости причиной нейропатической боли (НБ). Распространенность ДПН варьирует в зависимости от используемых диагностических критериев. Частота нейропатии, диагностируемой на основании симптомов, составляет около 25%, а при проведении электронейромиографического исследования — 100% у больных СД [2].
Диагноз ДПН основывается на тщательно собранном анамнезе, неврологическом обследовании, электрофизиологическом исследовании. Типичными симптомами являются ощущение «бегания мурашек», жжения, боли в голенях и стопах, ночные судороги мышц. При неврологическом обследовании выявляются ослабление ахилловых рефлексов, нарушение чувствительности по типу «носков» и «перчаток», снижение проприоцептивной чувствительности. При несвоевременно начатом лечении и неэффективности терапии развиваются такие осложнения ДПН, как язвы стоп, которые могут приводить к некрозу, гангрене (диабетическая стопа) и часто к ампутациям. Пациенты с СД нуждаются в ежегодном неврологическом и клиническом обследовании стопы [3].
Общепризнано, что основной причиной развития ДПН является повышенный уровень глюкозы [4]. Соответственно, единственным подтвержденным методом лечения, способным замедлять и даже в некоторой степени обращать прогрессирование ДПН, является хороший контроль уровня гликемии у больных с инсулинзависимым СД. У пациентов с интенсивной терапией СД (3 или более инъекции инсулина в день либо выполнение непрерывной подкожной инфузии инсулина с помощью дозатора инсулина (уровень HbA1c в диапазоне 6,5–7,5)) наблюдалось достоверное снижение риска развития микрососудистых осложнений и нейропатии [5]. Интенсивное лечение сульфонилмочевинами пациентов с инсулинонезависимым типом СД также приводило к снижению частоты и прогрессирования нейропатии [6]. Однако только достижение нормогликемии не способно быстро ликвидировать клинические проявления ДПН. В связи с этим требуется дополнительное патогенетическое и симптоматическое лечение, особенно для купирования болевого синдрома.
К препаратам патогенетического действия относится альфа-липоевая (тиоктовая) кислота (Эспа-липон, Тиоктацид, Тиогамма, Тиолепта). Эти препараты являются золотым стандартом патогенетического лечения ДПН. Альфа-липоевая кислота является мощным липофильным антиоксидантом. Тиоктовая кислота, накапливаясь в нервных волокнах, снижает содержание свободных радикалов; увеличивает эндоневральный кровоток; нормализует содержание NO, регулятора расслабления сосудистой стенки (если его много, как при СД, то он начинает действовать как свободный радикал); улучшает эндотелиальную функцию; снижает уровень общего холестерина, увеличивает уровень антиатерогенной фракции липопротеинов высокой плотности. В ряде исследований показано, что применение альфа-липоевой кислоты в дозе 600 мг/день в/в или перорально в течение от трех недель до шести месяцев уменьшает в клинически значимой степени главные симптомы ДПН, включая боль, парестезии и онемение [7, 8]. Оптимальным считается назначение в начале лечения внутривенного капельного введения альфа-липоевой кислоты (600 мг на 200 мл физиологического раствора) в течение 3 недель (15 капельниц) с последующим приемом 600 мг препарата в виде таблеток (один раз в день за 30–40 минут до еды) в течение 1–2 месяцев.
К препаратам, которые улучшают метаболизм пораженных нервных структур, традиционно относятся витамины группы B, что обусловлено их нейротропными свойствами. Витамин B1 участвует в синтезе ацетилхолина, а В6 — в синтезе нейромедиаторов, передаче возбуждения. Витамин В12 улучшает трофику периферических нервов. Показана высокая эффективность препарата Мильгамма драже в комплексном лечении ДПН. В его состав входят 100 мг бенфотиамина и 100 мг пиридоксина. Препарат назначается по одному драже 2–3 раза в сутки в течение 3–5 недель. Важно, что Мильгамма содержит бенфотиамин, липидорастворимость которого является причиной достижения высокой концентрации тиамина в крови и тканях.
Данные об эффективности и профиле безопасности позволяют рассматривать альфа-липоевую кислоту и бенфотиамин как препараты первой линии патогенетически ориентированной терапии диабетической полинейропатии [9].
В двух мультицентровых плацебо-контролируемых исследованиях 1335 пациентов с ДПН показано, что прием ацетил-L-карнитина в дозе 1000 мг 3 раза в день в течение 6 и 12 месяцев значительно уменьшал симптоматику ДПН [10].
Направление патогенетической терапии является чрезвычайно важным и во многом предопределяет прогноз. Однако лечение проводится длительными курсами и не всегда сопровождается быстрым очевидным клиническим улучшением. В то же время даже при негрубой ДПН может иметь место выраженный болевой синдром, приводя к нарушениям сна, депрессии, тревоге и социальной дезадаптации. Именно поэтому параллельно с патогенетической терапией чрезвычайно важно проводить своевременную симптоматическую терапию НБ.
Хочется сразу подчеркнуть, что простые анальгетики и нестероидные противовоспалительные препараты в лечении болей при ДПН не рекомендуются из-за их неэффективности [11]. К сожалению, в мире более 60% больных с НБ по-прежнему получают эти препараты, что недопустимо и чрезвычайно опасно при длительном применении (осложнения со стороны желудочно-кишечного тракта (ЖКТ), печени и крови). Основными группами препаратов для лечения НБ при ДПН являются: антидепрессанты, антиконвульсанты, опиоиды, антиаритмические средства, средства местного действия.
Трициклические антидепрессанты (ТЦА) стали одними из первых препаратов, которые продемонстрировали свою эффективность в лечении пациентов с НБ [12]. Тем не менее в России зарегистрирован только один ТЦА — амитриптилин, который используется для лечения НБ (постгерпетическая невралгия, ДПН). Считается, что обезболивающее действие ТЦА связано с ингибированием ими обратного захвата серотонина и норадреналина, следствием чего является усиление нисходящей активности норадренергических и серотонинергических систем, оказывающих тормозящее влияние на проведение болевых импульсов по ноцицептивным путям в ЦНС.
Помимо блокирования обратного захвата серотонина и норадреналина ТЦА блокируют альфа1-адренергические, Н1-гистаминовые, М-холинергические рецепторы, что обусловливает целый ряд противопоказаний и побочных эффектов, ограничивающих их применение. Среди побочных эффектов наблюдаются нарушение зрения, сухость во рту, синусовая тахикардия, запор, задержка мочи, спутанность сознания и/или нарушение памяти (антихолинергические эффекты); седативный эффект, сонливость, увеличение веса (Н1-гистаминовые эффекты); ортостатическая гипотензия, головокружение, тахикардия (альфа1-адренергические эффекты) [13]. ТЦА противопоказаны больным с острым и подострым инфарктом миокарда, с нарушением внутрижелудочковой проводимости, с закрытоугольной глаукомой, принимающими ингибиторы моноаминоксидазы (ИМАО). Эти препараты следует применять с осторожностью пациентам с ишемической болезнью сердца (ИБС), аритмией, артериальной гипертонией, после инсульта, а также с задержкой мочи или вегетативной недостаточностью. Данное обстоятельство существенно ограничивает применение ТЦА в общемедицинской практике.
Эффективность применения ТЦА (амитриптилин, дезипрамин, кломипрамин, имипрамин) при лечении болевой формы ДПН показана в ряде рандомизированных плацебо-контролируемых исследований [14]. Наиболее распространенными препаратами этой группы, применяемыми для лечения болевых полинейропатий, являются амитриптилин и имипрамин [15]. Наиболее широко используется амитриптилин. Начальная доза препарата составляет 10–12,5 мг на ночь, затем дозу постепенно увеличивают на 10–25 мг каждые 7 дней до достижения эффекта (максимально до 150 мг/сут). Суточную дозу принимают однократно на ночь или дробят на 2–3 приема. При сопутствующей депрессии обычно требуется назначение более высоких доз препарата. При непереносимости амитриптилина возможно назначение других ТЦА, например имипрамина или кломипрамина. Пробное лечение антидепрессантами должно продолжаться как минимум 6–8 недель, при этом максимально переносимую дозу пациент должен принимать не менее 1–2 недель. Хотя амитриптилин эффективен примерно у 70% больных с НБ, выраженные побочные эффекты ограничивают его применение. Перед назначением любого ТЦА обязательно предварительное проведение ЭКГ, особенно у лиц старше 40 лет.
При плохой переносимости ТЦА возможно применение тетрациклических антидепрессантов (например, мапротилина, 25–100 мг/сут) или селективных ингибиторов обратного захвата серотонина и норадреналина (СИОЗСН) (венлафаксина, 150–225 мг/сут, или дулоксетина, 60–120 мг/сут) [16]. Эффективность венлафаксина неоднократно доказана в ходе исследований, включавших пациентов с ДПН [17, 18], при этом у него отсутствуют постсинаптические эффекты, свойственные для ТЦА (действие на М-холинорецепторы, альфа-адренергические и гистаминовые рецепторы). Это делает препарат более безопасным, чем ТЦА. Наступление противоболевого эффекта отмечено уже на второй неделе терапии [19].
Таким образом, венлафаксин является эффективным, безопасным, хорошо переносимым лекарственным средством при лечении ДПН. В трех мультицентровых рандомизированных двойных слепых плацебо-контролируемых исследованиях длительностью от 12 до 13 недель показана эффективность применения дулоксетина в дозе от 60 до 120 мг/сут у больных с болевой ДПН. В результате исследований обнаружено 50% снижение интенсивности боли при лечении дулоксетином (вне зависимости от применяемой дозы) у 41% больных, по сравнению с 24% пациентов, принимавших плацебо [20].
Селективные ингибиторы обратного захвата серотонина (СИОЗС) (флуоксетин, пароксетин, сертралин, циталопрам, эсциталопрам) вызывают меньше побочных действий, но оказывают менее отчетливый противоболевой эффект, что, возможно, объясняется отсутствием прямого влияния на норадренергическую передачу. Они показаны, главным образом, в тех случаях, когда боль связана с депрессией, а больной плохо переносит другие антидепрессанты [16].
Поскольку НБ часто сопровождается депрессией, актуальным является выбор препарата, эффективно воздействующего на это психопатологическое состояние и обладающего хорошим профилем безопасности. Одним из таких препаратов является пипофезин (Азафен) [21]. Механизм антидепрессивного действия основан на неизбирательном ингибировании обратного захвата серотонина и норадреналина, что приводит к увеличению их концентрации в ЦНС. Препарат не обладает кардиотоксическими свойствами. В связи с отсутствием холинолитического действия Азафен можно назначать больным глаукомой и другими заболеваниями, при которых противопоказано применение препаратов, обладающих холинолитической активностью, в том числе имипрамина и амитриптилина. Отсутствие выраженных побочных явлений позволяет назначать препарат больным с соматическими заболеваниями и лицам пожилого возраста, прежде всего, в амбулаторной практике.
Среди антиконвульсантов, применяемых при лечении болевой ДПН, наиболее эффективными являются габапентин (Нейронтин) и прегабалин (Лирика) [22, 23]. Механизм действия габапентина и прегабалина, по-видимому, основан на способности связываться с альфа-2-дельта-субъединицами потенциалзависимых кальциевых каналов периферических сенсорных нейронов. Это приводит к снижению входа кальция в пресинаптический нейрон, в результате чего уменьшается высвобождение главных медиаторов боли (глутамата, норадреналина и субстанции Р) перевозбужденными нейронами, что сопровождается редукцией болевого синдрома. Оба препарата обладают хорошей переносимостью и высокой эффективностью, наблюдаемой уже на 1-й неделе лечения. Наиболее частыми побочными эффектами являются головокружение и сонливость. Начальная доза габапентина — 100–300 мг на ночь. Затем суточную дозу постепенно увеличивают каждые 3–5 дней на 100–300 мг, переходя на трехкратный прием.
Средняя эффективная доза составляет 1800 мг/сут (600 мг 3 раза в день), максимальная — 3600 мг/сут. На титрование дозы габапентина может уйти от 2 до 8 недель. Прежде чем делать вывод о неэффективности препарата, его максимально переносимую дозу следует принимать 1–2 недели. По показателям эффективности и безопасности прегабалин примерно соответствует габапентину, но в отличие от габапентина обладает линейной фармакокинетикой, что обеспечивает предсказуемость изменений концентрации препарата в плазме крови при изменении дозы. Диапазон суточных доз преагабалина — 150–600 мг/сут в 2 приема.
При лечении болевой ДПН стартовая доза может составлять 150 мг/сут. В зависимости от эффекта и переносимости дозу можно увеличить до 300 мг/сут через 3–7 дней. При необходимости можно увеличить дозу до максимальной (600 мг/сут) через 7-дневный интервал. В соответствии с опытом применения препарата, при необходимости прекращения приема рекомендуется постепенно снижать дозу в течение недели. Прегабалин быстрее всасывается в кровь и обладает более высокой биодоступностью (90%) по сравнению с габапентином (33–66%). Вследствие этого препарат эффективен в меньших дозах и обладает меньшей частотой и выраженностью побочных эффектов, в особенности седации [22, 23].
Использование опиоидов для лечения болевых синдромов возможно только при отсутствии эффекта от других препаратов. Среди опиоидов наиболее эффективными при лечении болевой ДПН оказались оксикодон в дозе 37–60 мг/сут [24] и трамадол (препарат, обладающий низкой аффинностью к опиоидным μ-рецепторам и одновременно являющийся ингибитором обратного захвата серотонина и норадреналина). Лечение трамадолом начинают с дозы 50 мг на ночь (или 25 мг 2 раза в день), спустя 5–7 дней дозу увеличивают до 100 мг/сут. При необходимости дозу повышают до 100 мг 2–4 раза в день. Пробное лечение трамадолом должно продолжаться не менее 4 недель [25]. Опиоиды ценятся за их болеутоляющие свойства, но препараты этого класса вызывают в организме и чрезвычайно выраженные и опасные побочные эффекты.
Комбинация трамадола с парацетамолом (Залдиар) позволяет снизить дозу трамадола и тем самым риск побочного действия, не жертвуя анальгетическим эффектом [26]. При комбинации двух указанных препаратов, обладающих разным механизмом действия (механизм анальгетического эффекта парацетамола может быть связан с ингибирующим эффектом на центральный синтез простагландинов, возможно, за счет торможения ЦОГ-3), возникает эффект синергизма. Адекватное обезболивание при приеме комплекса препаратов наблюдается в 1,5–3 раза чаще, чем при применении каждого из соединений в соответствующих дозах.
Кроме того, для парацетамола и трамадола характерен взаимодополняющий фармакокинетический профиль, благодаря которому препарат быстро начинает действие — уже через 15–20 минут (за счет парацетамола) и длительное время поддерживает анальгетический эффект (за счет трамадола) [26]. В состав Залдиара входит низкая доза трамадола (в одной таблетке содержится 37,5 мг трамадола и 325 мг парацетамола), поэтому побочные эффекты при его применении возникают реже, чем при применении трамадола. Назначение препарата не требует длительного титрования дозы, лечение может быть начато с дозы 1–2 таблетки в день, в последующем доза может быть повышена до 4 таблеток в сутки.
Пероральный антиаритмический препарат мексилетин также относится к анестетикам. Считается, что мексилетин блокирует натриевые каналы, таким образом стабилизируя мембрану нейронов и блокируя передачу болевых импульсов. Испытания по применению мексилетина при НБ дают противоречивые результаты. В ряде случаев мексилетин значительно уменьшает боль, особенно при его применении в высоких дозах. Однако при этом чаще возникают побочные эффекты, в частности со стороны ЖКТ. Препарат следует применять с осторожностью при наличии в анамнезе сердечной патологии или выявлении нарушений при ЭКГ-исследовании [27].
В ряде исследований было показано, что применение местных анестетиков (кремов, гелей и пластыря (Версатис) с 5-процентным содержанием лидокаина или препаратов на основе экстрактов жгучего перца — капсаицина) было эффективным при лечении болевой формы ДПН [27, 28]. Эффект лидокаина основан на блокировании транспорта ионов натрия через мембрану периферических нейронов, в результате чего происходит стабилизация клеточной мембраны, замедляется распространение потенциала действия, а следовательно, уменьшается боль. Из побочных эффектов может наблюдаться местное раздражение кожи в области нанесения, которое чаще всего незначительно и быстро проходит. Действие препаратов капсаицина основано на истощении запасов субстанции Р в терминалях сенсорных волокон. Жжение, покраснение и зуд в месте нанесения являются наиболее частыми побочными эффектами, часто отмечается усиление боли при первом нанесении препарата.
Тем не менее ни одно лекарственное средство нельзя рассматривать в качестве единственного препарата для лечения боли при ДПН [29]. Нередки случаи, когда применение любого из перечисленных выше средств оказывается недостаточно эффективным и возникает потребность в комбинации препаратов. Поэтому хотя число одновременно принимаемых пациентом лекарственных средств по общему правилу следует стараться ограничивать, но в большинстве случаев НБ при ДПН удается адекватно контролировать лишь с помощью комбинации двух и более препаратов. Нерационально сразу же назначать комбинацию нескольких средств: первоначально следует испробовать один препарат, и лишь убедившись, что в переносимых данным пациентом дозах он оказывает лишь частичный эффект, к нему следует присоединить следующее средство, которое, как правило, обладает иным механизмом действия.
В клинической практике часто комбинируют антидепрессант с антиконвульсантом, антиконвульсант с трамадолом или Залдиаром. Рекомендуется избегать сочетания трамадола (особенно больших доз) с ИМАО, СИОЗС и СИОЗСН, так как подобная комбинация может спровоцировать серотониновый синдром. С осторожностью трамадол следует назначать в комбинации с трициклическими антидепрессантами (учитывая риск серотонинового синдрома) [30].
Нефармакологические методы лечения ДПН включают в себя психотерапию, бальнеотерапию, гипербарическую оксигенацию (1,2–2 атм.), фототерапию, магнитотерапию, электрофорез, диадинамические токи, электростимуляцию паретичных мышц, чрескожную электронейростимуляцию, иглорефлексотерапию. Противопоказанием к их применению является тяжелое состояние больного, обусловленное соматической патологией и/или тяжелая декомпенсация метаболизма. Рядом авторов показана высокая эффективность электростимуляции спинного мозга, используемой для лечения болевой диабетической нейропатии [31]. Как правило, имплантацию стимуляторов производят у пациентов с рефрактерными к фармакотерапии болевыми синдромами.
В заключение следует заметить, что лечение каждого пациента должно быть индивидуальным с учетом клинических особенностей, а также наличия коморбидных заболеваний (тревоги, депрессии, заболеваний внутренних органов и т. д.). При выборе лекарственных препаратов, помимо непосредственного анальгетического эффекта, должны быть учтены другие положительные эффекты выбранного препарата (уменьшение уровней тревоги, депрессии, улучшение сна и настроения), а также его переносимость и возможность развития серьезных осложнений.
Ряд авторов в качестве препаратов первого ряда при лечении болевых форм полинейропатий рекомендуют ТЦА и габапентин или прегабалин. К препаратам второго ряда относят СИОЗСН — венлафаксин и дулоксетин. Они обладают меньшей эффективностью, но более безопасны, имеют меньше противопоказаний по сравнению с ТЦА, и им должно быть отдано предпочтение при лечении больных с сердечно-сосудистыми факторами риска. Препараты третьей линии включают в себя опиоиды. К препаратам с более слабым эффектом относятся капсаицин, мексилетин, окскарбазепин, СИОЗС, топиромат, мемантин, миансерин [32].
Литература
*Первый МГМУ им. И. М. Сеченова, **МОНИКИ им. М. Ф. Владимирского, Москва