Стандарты лечения болезни Паркинсона
Лечение при появлении моторных флуктуаций и/или дискинезий
Уменьшение длительности действия средств, содержащих леводопу. При усилении симптомов паркинсонизма к концу действия очередной дозы средства, содержащего леводопу, прибегают к одной из следующих мер:
Если выбранная мера оказалась неэффективной, следует применить комбинацию препаратов (уровень С).
Замедленное наступление или отсутствие эффекта разовой дозы средства, содержащего леводопу. Если отдельные дозы препарата леводопы, принятые в течение дня, оказываются неэффективными, рекомендуют:
Непредсказуемые колебания эффекта разовой дозы средств, содержащих леводопу, в течение дня (синдром «включения-выключения»). При появлении эпизодов внезапного усиления симптомов паркинсонизма на фоне действия очередной дозы леводопы следует предпринять следующее:
Кроме того, показаны меры, аналогичные рекомендуемым, при замедленном наступлении или отсутствии эффекта разовой дозы средства, содержащего леводопу.
Насильственные движения на высоте действия разовой дозы средства, содержащего леводопу (дискинезия пика дозы). Если на высоте действия препарата леводопы появляются насильственные движения, ограничивающие жизнедеятельность пациента, нужно предпринять следующие действия:
Насильственные движения в начале и конце действия разовой дозы средства, содержащего леводопу (двухфазные дискинезии). При двухфазных дискинезиях нужно предпринять следующие меры:
Дистония, вызванная прекращением действия очередной дозы средства, содержащего леводопу. При болезненных дистониях, вызываемых прекращением действия очередной дозы средства, содержащего леводопу, необходимы следующие меры:
Если, несмотря на коррекцию схемы приема противопаркинсонических средств, сохраняются непроизвольные движения или нестабильность эффекта средств, содержащих леводопу, которые существенно ограничивают жизнедеятельность пациента (снижают трудоспособность или возможность самообслуживания), показана консультация нейрохирурга, специализирующегося в стереотаксической нейрохирургии, для решения вопроса о целесообразности нейрохирургического вмешательства.
Лечение нарушений сна
При пробуждениях, вызванных усилением симптомов паркинсонизма в ночное время (ночная акинезия), прибегают к одной из следующих мер:
При ночной акатизии уменьшают вечернюю дозу средства, содержащего леводопу (уровень С), а если эта мера оказывается недостаточной, то на ночь назначают клоназепам (уровень С). При неэффективности указанных мер дополнительно назначают золпидем, 10–20 мг на ночь (уровень С), антидепрессант с седативным действием (тразодон — 75–150 мг, амитриптилин — 25–50 мг или миртазапин — 15–30 мг) (уровень С).
Лечение больных БП с нарушением познавательных функций
Ухудшение познавательных функций требует в первую очередь оптимизации противопаркинсонической терапии с обеспечением адекватного уровня двигательных функций. Основным противопаркинсоническим средством у больных с выраженными познавательными нарушениями должны быть препараты, содержащие леводопу, которые у этой категории больных реже вызывают побочные эффекты (уровень С). Назначение антихолинергических средств противопоказано в связи с высоким риском ухудшения психических функций и развития психотических расстройств (уровень В).
Кроме того, при ухудшении познавательных функций необходимы:
Для улучшения познавательных функций у больных БП с деменцией могут применяться:
Консультация психиатра и наблюдение за больными с психическими нарушениями показаны при развитии тяжелых психотических расстройств (депрессии, психопатоподобные нарушения, галлюциноз, параноидный синдром, делирий).
При зрительных галлюцинациях на фоне ясного сознания, сохранности ориентации и критики проводится плановая коррекция противопаркинсонической терапии (уровень В). В первую очередь снижают дозу или отменяют недавно назначенное или наименее эффективное средство (уровень В), часто в следующем порядке: холинолитик — селегилин — амантадин — агонист дофаминовых рецепторов — ингибитор КОМТ (уровень С).
При сохранении галлюцинаций следует снизить дозу средства, содержащего леводопу, до минимального эффективного уровня, обеспечивающего необходимый уровень двигательной активности (уровень В). При неэффективности этой меры или невозможности снизить дозу средства, содержащего леводопу, из-за нарастания двигательного дефекта назначается клозапин в дозе от 6,25 до 50 мг на ночь (уровень В); после регресса галлюциноза препарат постепенно отменяют в течение 2–3 нед (уровень С). В течение всего срока лечения клозапином необходимо 1 раз в неделю исследовать содержание лейкоцитов в крови. При снижении их уровня ниже 3 тыс./мкл препарат должен быть отменен.
При неэффективности или непереносимости клозапина вместо него может быть назначен кветиапин, 25–200 мг/сут (уровень С), ингибитор холинэстеразы (уровень С).
При сочетании зрительных галлюцинаций с бредовыми нарушениями или при их возникновении на фоне спутанности сознания с развитием делирия необходимо, помимо указанных выше мер, следующее:
Следует избегать назначения на ночь бензодиазепинов с длительным действием (диазепам, хлордиазепоксид и т. д.), способных спровоцировать спутанность сознания.
Лечение акинетического криза
Акинетический криз — внезапное стойкое усиление гипокинезии и ригидности с развитием обездвиженности и нарушения бульбарных функций (дизартрии и дисфагии), возникающее спонтанно или связанное с прекращением приема, снижением дозы средств, содержащих леводопу, нарушением их всасывания в желудочно-кишечном тракте, развитием интеркуррентной инфекции.
Лечение осуществляется в условиях стационара. Проводится исследование причин акинетического криза (прекращение приема или снижение дозы противопаркинсонических средств, заболевание желудочно-кишечного тракта, вызывающее нарушение всасывания препаратов леводопы, интеркуррентная инфекция, цереброваскулярное заболевание, декомпенсация соматического заболевания).
Лекарственная терапия назначается индивидуально на основании данных анамнеза и ежедневного осмотра пациента. При дисфагии необходимо введение назогастрального зонда для кормления и введения лекарств. Показан комплекс мер по предупреждению пролежней, прежде всего повороты в постели каждые 2 ч, регулярная обработка мест костных выступов камфорным спиртом, использование противопролежневых матрасов.
Если акинетический криз возник в результате внезапного прекращения приема средства, содержащего леводопу, то его следует назначить вновь в более низкой дозе (50–100 мг 3–4 раза в сутки), затем постепенно увеличивать дозу каждые 3 дня до получения эффекта (но не более чем до 700–800 мг леводопы в сутки) (уровень С).
Если акинетический криз возник вследствие снижения дозы, то ее следует увеличить на 100 мг каждые 3 сут до достижения эффекта (но не более чем до 700–800 мг леводопы в сутки) (уровень С).
При дисфагии (но при нормальной функции желудочно-кишечного тракта) препараты леводопы вводят в растворенном виде через зонд.
В качестве дополнительного средства, особенно при нарушении глотания и всасывания препаратов в желудочно-кишечном тракте, назначают амантадина сульфат — 200 мг/500 мл в/в капельно со скоростью 60 капель в 1 мин 1–2 раза в сутки в течение 5–10 дней (уровень С) с последующим обязательным переходом на прием амантадина внутрь (100–200 мг 3 раза в день).
При дегидратации с целью достижения эуволемии вводят физиологический раствор, раствор Рингера, 0,45% раствор хлорида натрия и 5% раствор глюкозы, раствор альбумина, Реополиглюкин (уровень С).
Для профилактики тромбоза глубоких вен голени и тромбоэмболических осложнений показано назначение прямых антикоагулянтов (Гепарин, 2,5–5 тыс. единиц подкожно 2 раза в день или Фраксипарин 0,3 мл подкожно 2 раза в сутки) до разрешения акинетического криза (уровень С).
До восстановления глотания питание проводится через назогастральный зонд. При нарушении функции желудочно-кишечного тракта проводится парентеральное питание.
При появлении дыхательной недостаточности, острой сердечной недостаточности и тяжелой дисфагии, создающей угрозу аспирации, больной переводится в отделение интенсивной терапии, где проводится интубация, а при необходимости и искусственная вентиляция легких. Реабилитация, включающая лечебную гимнастику и массаж, осуществляется после купирования криза и стабилизации состояния.
По вопросам литературы обращайтесь в редакцию.
О. С. Левин, доктор медицинских наук, профессор
РМАПО, Центр экстрапирамидных заболеваний, Москва
Болезнь Паркинсона: как с ней справляться
Рисунок 1. Применение антихолинергических препаратов, известных с прошлого века, для снятия тремора и ригидности ограничено из-за их побочных эффектов Каковы основные диагностические критерии болезни Паркинсона? Когда пациента необходимо
 |
| Рисунок 1. Применение антихолинергических препаратов, известных с прошлого века, для снятия тремора и ригидности ограничено из-за их побочных эффектов |
Каковы основные диагностические критерии болезни Паркинсона?
Когда пациента необходимо отправить к специалисту?
С каких препаратов начать лекарственную терапию?
Каким образом устранить побочное действие специфической терапии?
Причины паркинсонизма до сих пор неизвестны, а лечение остается симптоматическим, несмотря на то, что прошло уже четверть века с тех пор, как леводопа прочно внедрилась в жизнь больных паркинсонизмом.
Но не будем слишком пессимистичны — современные методы лечения продлевают жизнь таким больным и делают ее более или менее нормальной [1]. Один человек из тысячи страдает болезнью Паркинсона. Диагноз ставится на основании клинического синдрома, включающего гипокинезию, ригидность, тремор и нарушенные рефлексы позы. Уровень допамина снижается почти на 80% к моменту появления клинических признаков, поэтому неудивительно, что невозможно точно указать время появления первых симптомов.
Далеко не всегда просто отличить идиопатическую болезнь Паркинсона от других состояний, включая такое часто встречающееся, как эссенциальный тремор, и менее распространенные заболевания, которым присущи иные неврологические симптомы — супрануклеарный паралич, автономные нарушения или мозжечковые симптомы [2].
Патолого-анатомические исследования показывают, что каждый пятый диагноз в данной группе заболеваний ошибочен. Перед тем как поставить диагноз, важно убедиться в наличии по крайней мере двух из четырех основных клинических признаков, помня при этом, что у большинства пациентов симптоматика асимметрична. В сомнительных случаях помогает пробное лечение леводопой или допаминовыми агонистами [3].
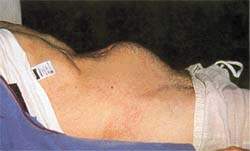 |
| Рисунок 2. Задержка мочи часто сопровождает болезнь Паркинсона |
Основной проблемой в контролировании болезни Паркинсона на сегодняшний день остается поздняя недостаточность допаминергической терапии, проявляющаяся в исчезновении или колебаниях реакции на препарат или в развитии дискинезий и прочих побочных эффектов у 75% пациентов после пяти лет лечения [4].
Расширение спектра препаратов и вновь возросший интерес к хирургическому лечению объясняется стремлением избежать или уменьшить проблемы длительного лечения.
Врач общей практики, подозревающий у пациента болезнь Паркинсона, должен решить, к кому его направить — к невропатологу, гериатру или другим специалистам. Особенно это важно в хронических прогрессирующих случаях у молодых людей, нуждающихся в длительном лечении.
Пациенту крайне необходимо рассказать о его болезни, прогнозе и сути применяемого лечения. Как и при астме, диабете и другом хроническом заболевании, врач и пациент должны действовать сообща, при активном участии последнего в принятии решений, касающихся лечения.
Как правило, с такими пациентами легко договориться, но по мере прогрессирования заболевания их приходится уговаривать принимать различные препараты несколько раз в день.
Контроль за заболеванием не сводится лишь к лекарственной терапии, напротив, психотерапия, трудотерапия, обучение навыкам речи и психологические методы существенно улучшают состояние пациентов [5]. Регулярная физиотерапия, назначаемая до допаминергических препаратов, замедляет прогрессирование заболевания [6], поэтому сразу после установления диагноза нужно советовать пациентам физические упражнения, соблюдение диеты, трудотерапию.
Весьма часто такие методы используются на более поздних стадиях заболевания, когда ничто другое уже не помогает, в то время как их нужно использовать для предупреждения развития болезни. Общество больных болезнью Паркинсона выпускает информационные сборники для персонала больниц и специальный обучающий материал для пациентов.
В ряде центров специально обученные сиделки помогают больным и тем, кто за ними ухаживает. Несмотря на отсутствие конкретных научных данных, многие пациенты признают эффект музыкотерапии, обучения, йоги и прочих дополнительных методов лечения.
Количество доступных препаратов и их новых форм в последние десять лет значительно увеличилось и обещает еще большее увеличение в ближайшем будущем. В табл. 1 приведены основные группы препаратов.
Таблица 1. Лекарственные препараты, применяемые для лечения паркинсонизма
антихолинергические препараты
Антихолинергические средства применялись еще в прошлом веке. Они до сих пор помогают справиться с тремором и, в меньшей степени, с ригидностью, практически не влияя на гипокинезию. Выбор среди них невелик. Все они имеют побочные эффекты: сухость во рту, нарушение аккомодации, запор и задержка мочи. У пожилых пациентов они склонны вызывать спутанность сознания и прочие психиатрические нарушения.
Следует отметить, что все антипаркинсонические средства способны вызывать подобные проблемы и любое нарушение ментальной функции требует пересмотра целесообразности применения и адекватности доз препарата. Леводопа, в настоящее время назначаемая вместе с ингибитором периферической декарбоксилазы (ИНД), остается пока самым эффективным лекарственным средством. В начале курса лечения могут возникать тошнота, рвота, поэтому пациенты предпочитают принимать их вместе с пищей или с противорвотными лекарствами — домперидоном и метоклопрамидом.
Необходимо учитывать, что большое потребление белка может мешать всасыванию леводопы.
Кроме психологических расстройств необходимо отметить и другие побочные эффекты — дискинезии или непроизвольные движения. Они бывают различными: движения языка и губ, гримасы, болезненные напряжения мышц, хореоатетоз, двигательное беспокойство. Снижение дозы препарата, как правило, уменьшает и дискинезию, однако пациенты часто предпочитают последнюю невозможности передвигаться вообще.
Другой элемент нарушений, возникающих при длительном лечении, — колебания реакции на препарат. Вначале это проявляется феноменом «выключения» — продолжительность действия леводопы-ИПД все время уменьшается. В тяжелых случаях человек внезапно переключается от движения, обычно с дискинезиями, к полной неподвижности.
 |
| Рисунок 3. Нарушение постуральных рефлексов — одна из составляющих клинического синдрома |
Для преодоления подобных проблем были разработаны формы с дозированным высвобождением препарата, позволяющие избежать колебаний концентраций лекарства в крови, и порошковые формы, обеспечивающие быстрое нарастание уровня лекарства в крови.
Агонисты допамина действуют на различные участки дофаминового рецептора. Соответственно разнится и их действие. Применяемые в одиночку, агонисты допамина менее эффективны, чем леводопа, но и реже приводят к колебаниям и дискинезиям [4]. Желудочно-кишечные побочные эффекты и воздействие на психику у них такие же. Апоморфин отличается от прочих упомянутых средств тем, что вводится путем инъекции.
По данным исследования, проведенного в Соединенных Штатах, селигин отсрочивает необходимость назначения леводопы, имеет нейропротекторные свойства и способен замедлять развитие болезни [7]. С тех пор, однако, было доказано, что селегилин сам по себе обладает умеренным допаминергическим эффектом, а также амфетаминоподобным и антидепрессантным воздействием; его защитные свойства в настоящее время находятся под сомнением [8].
Механизм действие селегилина — блокада моноаминоксидазы В, одного из основных ферментов допаминового метаболизма. Бытует мнение, что он потенциирует действие леводопы.
Ингибиторы катехол-о-метилтрансферазы (КОМТ) просто замедляют метаболизм допамина. По крайней мере два таких препарата уже готовятся к массовому производству [9, 10].
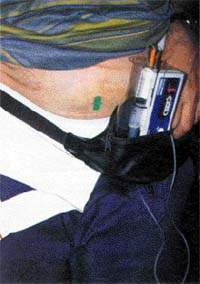 |
| Рисунок 4. Инъекции апоморфина применяют в трудно поддающихся лечению случаях |
Допаминергический эффект антивирусного препарата амантадина замечен еще много лет назад, но он менее эффективен, чем леводопы. Точный механизм его действия неизвестен, но все же его пытаются применять в случаях, резистентных к терапии леводопой; кроме того, его назначение совместно с леводопой позволяет уменьшить дозу последней.
Бесспорно, при назначении лекарственных препаратов следует учитывать возраст пациента, степень нарушений и индивидуальные особенности, однако невропатологи, как и другие специалисты, единого подхода к последовательности применения препаратов пока не разработали. Некоторые считают, что откладывать применение леводопы не имеет смысла, и начинают со стандартных схем ее использования.
Еще один подход заключается в использовании сначала пролонгированных форм, применении только дофаминового агониста или в сочетании с низкими дозами леводопы; или же назначают на какое-то время один селегилин, а затем присоединяют леводопу.
Какой бы схеме вы ни следовали, целесообразно начинать с низких доз, осторожно и постепенно подбирая необходимую дневную дозу. По возможности нужно избегать резких изменений в схеме приема или быстрого увеличения дозы.
При развитии феномена «выключения» нередко, хотя и на непродолжительное время, может оказаться полезным разделение дневной дозы препарата на несколько более мелких приемов. Можно попробовать присоединить к леводопе селегилин и/или агонист допамина, а также использовать вместо леводопы (или чаще дополнительно к ней) лекарственные формы пролонгированного действия. Биодоступность подобных форм меньше, чем у обычных препаратов, и их доза обычно несколько больше. У отдельных пациентов хороший результат дает прием препарата до, а не после еды или сокращение потребления белка.
В случаях с ярко выраженным феноменом включения-выключения используют те же приемы, в сочетании с индивидуальным подбором наиболее эффективной схемы лечения.
| Не рекомендуется устраивать длительные перерывы между приемами препаратов |
При отсутствии успеха от перорального приема препарата можно использовать такие новые методы, как подкожное введение апоморфина. Правда, для этого требуется обученный персонал, лучше всего — специальная сиделка для больных паркинсонизмом.
Другой подход — нейрохирургия. Проводят стереотоксическую паллидотомию или стимуляцию таламуса при феномене включения-выключения, а также при упорном треморе [11]. Имеющиеся на сегодняшний день данные обнадеживают. Они свидетельствуют об уменьшении дискинезии и удлинении периода включения. Однако, как и трансплантацию фетальных тканей, подобные хирургические методы пока следует считать экспериментальными, требующими дальнейшего изучения и оценки.
Кроме дискинезий и тремора, у многих пациентов при прогрессировании заболевания развиваются когнитивные и психические расстройства. При этом необходимо снижать дозу препарата.
Небольшие перерывы в приеме лекарств, отмена допаминергических препаратов на короткое время — такие «каникулы» (один-два дня каждую неделю) позволяют снизить психотоксичность [10]. Отмена препаратов на длительный срок не рекомендуется, поскольку может повлечь серьезные или даже необратимые нарушения способности двигаться.
Болезнь Паркинсона сопровождается нарушениями сна, депрессией, задержкой мочи, запорами, болями, расстройствами автономной нервной системы и сексуальными отклонениями. Все это поддается лекарственной коррекции. Просто надо дать возможность пациенту подробно описать все, что его беспокоит. Ограниченное время консультации вместе с тяжелыми проблемами общения, от которых страдают многие пациенты, могут быть преодолены посредством заранее подготовленного самим пациентом или сиделкой описания его состояния.
1. Clarke C. E. Mortality from Parkinson’s disease in England and Wales 1921-89. J. Neurol. Neurosurg Psychiatry 1993; 56:690-3.
2. Quinn N. Parkinsonism — recognition and differential diagnosis. BMJ 1995; 310:447-52.
3. Hughes A. J., Lees A. J., Stern G. M. Challenge test to predict the dopaminergic response in untreated Parkinson’s disease. Neurology 1991; 41:1723-5.
4. Marsden C. D. Parkinson’s disease. J. Neurol. Neurosurg Psychiat 1994; 57:672-81.
5. Patti F., Reggio A., Nicoletti F. et al. Effects of rehabilitation therapy on Parkinsonians’ disability and functional independence. J. Neurol. Rehab 1996; 10:223-231.
6. Doshay L. J. Method and value of physiotherapy in Parkinson’s disease. N. Eng. J. Med. 1962; 266:878-80.
7. Parkinson Study Group. Effects of tocopherol and deprenyl on the progression of disability in early Parkinson’s disease. N. Eng. J. Med. 1993; 328:176-83.
8. Jankovic J., Shoulson I., Weiner W. J. Early-stage Parkinson’s disease: to treat or not to treat. Neurology 1994; 44(suppl1):S4-S7.
9. Pouttinen H. M., Rinne U. K. A double-blind pharmocokinetic and clinical dose-response study of entacapone as an adjuvant to levadopa therapy in advanced Parkinson’s disease. Clin. Neuropharmac 1996; 19:283-96.
10. Stocchi F., Nordera G., Marsden C. D. Strategies for treating patients with advanced Parkinson’s disease with disastrous fluctuations and dyskinesias. Clin. Neuropharmac 1997; 20:95-115.
11. Obeso J. A., Guridi J., Delong M. Surgery for Parkinson’s disease. J. Neurol. Neurosurg. Psychiat 1997; 62:2-8.
Чем заменить циклодол при паркинсоне
Лекарственный паркинсонизм является одним из самых частых вариантов вторичного паркинсонизма. По данным эпидемиологических исследований, с приемом лекарственных средств можно связать от 4 до 22% всех случаев паркинсонизма [1, 3]. Именно лекарственный паркинсонизм должен в первую очередь исключить врач у больного с недавно развившимися гипокинезией, ригидностью или тремором. Большинство больных с лекарственным паркинсонизмом относятся к возрастной категории от 60 до 80 лет, в этом же возрасте часто встречаются и нейродегенеративные заболевания, проявляющиеся экстрапирамидной симптоматикой, что создает трудности в дифференциальной диагностике этих состояний [3, 8]. Хотя ключевое значение в диагностике лекарственного паркинсонизма приобретает тщательное выяснение лекарственного анамнеза, диагностическую значимость самого факта приема того или иного препарата нельзя переоценивать. Важную роль играет анализ особенностей клинических проявлений паркинсонизма [3, 12].
Препараты, вызывающие лекарственный паркинсонизм
Неоднократно сообщалось и о случаях развития паркинсонизма при приеме трициклических антидепрессантов и препаратов лития. Однако анализ этих публикаций показывает, что речь в них идет не столько о синдроме паркинсонизма, сколько о треморе постурального или постурально-кинетического характера, иногда довольно грубом и сопровождающемся феноменом «зубчатого колеса» [3, 19, 23].
Нейролептический паркинсонизм
Нейролептический паркинсонизм возникает у 10—25% принимающих нейролептики больных. Среди пациентов с шизофренией частота лекарственного паркинсонизма колеблется от 19 до 36% [14]. Значительную долю пациентов с лекарственным паркинсонизмом составляют пожилые лица, страдающие деменцией, у которых раннее выявление лекарственного паркинсонизма особенно затруднено [19, 23].
Вероятность развития паркинсонизма при приеме того или иного нейролептика прямо пропорциональна его способности блокировать дофаминовые D2-рецепторы и обратно пропорциональна его способности блокировать мускариновые (М) холинорецепторы и серотониновые 5-НТ2-рецепторы (см. табл. 1)
| Таблица1 |
| Таблица2 |