Почему азитромицин остается препаратом выбора при внебольничных инфекциях нижних дыхательных путей
Инфекционно-воспалительные заболевания дыхательных путей занимают первое место в структуре инфекционной патологии. Пневмония является наиболее частой инфекционной причиной смерти в мире.
Инфекционно-воспалительные заболевания дыхательных путей занимают первое место в структуре инфекционной патологии. Пневмония является наиболее частой инфекционной причиной смерти в мире. В России ежегодно около 1,5 млн человек переносят пневмонию. В связи с этим остается актуальной проблема рационального выбора антибактериального средства для лечения инфекций нижних дыхательных путей. Выбор препарата для антибактериальной терапии должен основываться на его спектре действия, охватывающем выделенный или предполагаемый возбудитель, чувствительный к данному антибиотику, фармакокинетических свойствах антибактериального средства, обеспечивающих его проникновение в терапевтической концентрации в соответствующие ткани, клетки и жидкости организма, данных о безопасности антибиотика (побочных эффектах, противопоказаниях и возможном нежелательном взаимодействии с другими лекарствами), характеристиках лекарственной формы, способе введения и режиме дозирования, обеспечивающих высокий комплаенс терапии, фармакоэкономических аспектах лечения [4, 6, 8].
Инфекции нижних дыхательных путей и принципы выбора антибиотика
При неспецифических внебольничных инфекциях выбор антибактериального препарата в большинстве случаев основывается на статистических данных о наиболее частых их возбудителях, а также сведениях о подтвержденной в контролируемых клинических исследованиях эффективности тех или иных антибиотиков при инфекциях известной этиологии. Вынужденно эмпирический подход к лечению связан с отсутствием возможности микробиологического исследования в амбулаторных лечебных учреждениях, длительностью бактериологической идентификации возбудителя и определения его чувствительности к антибиотикам (3–5 дней, а в случае «атипичных» патогенов и больше), невозможностью в ряде случаев получить биологический материал для посева или бактериоскопии (например, около 30% больных пневмониями имеют непродуктивный кашель, что не позволяет исследовать мокроту), трудностями в разграничении истинных возбудителей и сапрофитов (обычно микроорганизмов ротоглотки, попадающих в исследуемый материал). Сложности выбора лекарственного средства в амбулаторных условиях определяются также отсутствием полноценного наблюдения за течением заболевания и, следовательно, своевременной коррекции лечения при его неэффективности. Антибиотики по-разному проникают в различные ткани и биологические жидкости. Лишь некоторые из них хорошо проникают в клетку (макролиды, тетрациклины, фторхинолоны, в меньшей степени — клиндамицин и сульфаниламиды). Поэтому, даже если препарат in vitro проявляет высокую активность в отношении данного возбудителя, но не достигает в месте его локализации уровня, превышающего минимальную подавляющую концентрацию (МПК) для данного микроорганизма, клинического эффекта он не окажет, хотя микробная резистентность к нему будет вырабатываться. Не менее важным аспектом антибактериальной терапии является ее безопасность, особенно для амбулаторного больного, лишенного повседневного медицинского наблюдения. В амбулаторных условиях следует отдавать предпочтение пероральному приему антибиотиков. В педиатрической практике имеют значение органолептические свойства препарата. Для повышения исполняемости пациентом врачебных назначений режим дозирования антибиотика должен быть максимально простым, т. е. предпочтительнее препараты с минимальной кратностью приема и коротким курсом лечения.
Возбудители неспецифических внебольничных инфекций нижних дыхательных путей
Острые респираторные вирусные инфекции (ОРВИ), протекающие с синдромом бронхита, в ряде случаев, чаще в детском возрасте, могут осложняться присоединением бактериальной флоры с развитием острого бронхита. Возбудителями острого бактериального бронхита в детском возрасте являются пневмококк, микоплазма или хламидия, реже гемофильная палочка, моракселла или стафилококк. Острый бактериальный бронхиолит у детей вызывают моракселла, микоплазма и возбудитель коклюша. Острый гнойный трахеобронхит у взрослых в 50% случаев вызывает гемофильная палочка, в остальных случаях пневмококк, реже моракселла (5–8% случаев) или внутриклеточные микроорганизмы (5% случаев).
Среди бактериальных возбудителей обострений хронического бронхита главную роль играют Haеmophilus influenzae (30–70% случаев), Streptococcus pneumoniae и Moraxella catarrhalis. Для курильщиков наиболее характерна ассоциация H. influenzae и M. catarrhalis. В отягощенных клинических ситуациях (возраст старше 65 лет, многолетнее течение болезни — более 10 лет, частые обострения — более 4 раз в год, сопутствующие заболевания, выраженные нарушения бронхиальной проходимости — объем форсированного выдоха за первую секунду (ОФВ1)
С. В. Лукьянов, доктор медицинских наук, профессор ФГУ «Консультативно-методический центр лицензирования» Росздравнадзора, Москва
Боль в горле
Подбор ЛС для лечения тонзиллита
Роза Исмаиловна Ягудина, д. ф. н., проф., зав. кафедрой организации лекарственного обеспечения и фармакоэкономики и зав. лабораторией фармакоэкономических исследований Первого МГМУ им. И. М. Сеченова.
Евгения Евгеньевна Аринина, к. м. н., ведущий научный сотрудник лаборатории фармакоэкономических исследований Первого МГМУ им. И. М. Сеченова.
Одной из наиболее распространенных жалоб в осеннее-зимний и, как ни странно, в летний периоды является боль в горле. Причинами возникновения болезненных ощущений могут стать различные патогенетические процессы, происходящие в организме человека, а летом – еще и нарушение экологической обстановки (влажный, запыленный воздух, кондиционеры). Наиболее частыми разновидностями поражений горла являются ларингит, фарингит и тонзиллит. Последнее из перечисленных заболеваний – это воспаление небных миндалин. Тонзиллит является самой распространенной причиной болей в горле, более того, нередко воспаление имеет хроническую форму течения.
Причины и механизм возникновения тонзиллита
Боль в горле, как считают сами пациенты, всегда связана с переохлаждением. Однако этиология развития поражений ротоглотки весьма разнообразна: от бактерий до вирусов. Возникновение болевого синдрома в этих случаях практически всегда связано с поражением небных миндалин, располагающихся на боковых стенках ротоглотки – стыке респираторного и пищеварительного трактов. Миндалины имеют множество лакун, в которые открываются крипты, или мешки, имеющие дихотомическое деление и погруженные в глубину миндалин. Такое строение миндалин способствует скоплению в них различных экссудатов. Небные миндалины не имеют приводящих лимфатических сосудов, так как сами активно продуцируют лимфоциты. Также небные миндалины принимают активное участие в формировании местного и общего иммунитета.
NB! Нельзя путать ангину и хронический тонзиллит (точнее, его обострение, которое при схожих симптомах требует иного лечения).
Ангина – общее инфекционное заболевание, с острым воспалением компонентов лимфаденоидного глоточного кольца (чаще именно небных миндалин). Ангины разделяют на: первичные, вторичные и специфические.
Хронический тонзиллит – хронический воспалительный, периодически обостряющийся очаг инфекции в небных миндалинах с общей инфекционно-аллергической реакцией.
Механизм распространения инфекции – воздушно-капельный, в основном происходит при кашле, чихании, поцелуе, пользовании одной посудой, полотенцами и пр. Наиболее частой причиной развития хронического тонзиллита является β-гемолитический стрептококк группы А, другими возбудителями – St. Aureus, H. influenzae, M. Catarrhalis, N. Gonorrhoeae, C. haemolyticum, M. Pneumoniae, C. pneumoniae, Toxoplasma, анаэробы, аденовирусы, цитомегаловирусы, вирусы герпеса и др. Хронический тонзиллит не всегда является следствием перенесенной ангины. В большинстве случаев он развивается незаметно, маскируясь под другие заболевания (ОРВИ, стоматит и др.). При прогрессировании тонзиллита медленно происходит замещение паренхимы миндалин соединительной тканью, образуются инкапсулированные очаги некроза, в воспаление вовлекаются регионарные лимфатические узлы. Выделяют несколько форм и видов хронического тонзиллита с различными симптомами.
Наличием только местных признаков характеризуется тонзиллит простой формы (начальная стадия)
Также на этой стадии могут обостряться другие, не связанные с тонзиллитом заболевания, которые могут иметь серьезные последствия.
Токсико-аллергическая форма I (ТАФ I) – обусловлена неоднократно перенесенными ранее ангинами. Помимо местных признаков (таких же, как и на начальной стадии), развиваются общие токсико-аллергические явления:
Сопутствующие заболевания в этом случае такие же, как при простой форме, но они не имеют единой инфекционной основы с хроническим тонзиллитом.
Токсико-аллергическая форма II (ТАФ II) – характеризуется местными признаками, присущими простой форме, и общими токсико-аллергическими реакциями:
Сопутствующие заболевания могут быть такими же, как при простой форме (не связаны с инфекцией). Течение данной стадии хронического тонзиллита может сопровождаться развитием тяжелых осложнений: паратонзиллярного абсцесса, тонзиллогенного сепсиса и др.
Лечение тонзиллита
Как избавиться от тонзиллита? Небные миндалины играют большую роль в нормальном функционировании иммунной системы, поэтому лечение заболевания в первую очередь должно предусматривать восстановление защитных функций организма. Фармакотерапия хронического тонзиллита включает в себя комплекс мер, направленных на устранение бактериальный среды, купирование воспаления и устранение гнойных пробок со слизистой оболочки глотки. Лечение хронического тонзиллита проходит в соответствии с формой и фазой заболевания (острый тонзиллит, латентный).
NB! Консервативная терапия проводится на начальной стадии заболевания и ТАФ I вне периода обострения и не ранее 1 месяца после него. Больным с ТАФ II показана тонзилэктомия!
Принципы фармакотерапии хронического тонзиллита:
Иммуномодуляторы
Антисептики
Растворы для полоскания
Важным этапом лечения боли в горле является санация ротоглотки с помощью разнообразных антисептиков. Лучшим вариантом санации является систематическое (до 8–10 раз в сутки) полоскание горла при тонзиллите антисептическими и противовоспалительными растворами фурацилина, настойки листьев эвкалипта (оказывают противомикробное действие), календулы, прополиса (оказывают антисептическое и противовоспалительное действие), препаратами, содержащими НПВП средство бензидамин и т. п.
Упомянутый выше бензидамин выпускается не только в форме раствора, но и в виде спрея, обеспечивающего так называемую «точечную» санацию ротоглотки. Другие спреи, применяющиеся при боли в горле, содержат гексэтидин, повидон-йод, смеси камфоры, левоментола, хлоробутанол и масла эвкалипта.
Другой удобной местной формой санации горла являются таблетки для рассасывания и пастилки на основе тех же антисептиков (комбинация сухого экстракта шалфея с эфирным маслом, амбазон, хлоргексидин в комбинации с тетракаином и витамином C). Как правило, помимо обезболивающего эффекта, таблетки и леденцы оказывают бактерицидное, местно-анестетическое и иммуномодулирующее действие. Основой для местных препаратов для рассасывания также могут быть препараты группы ПНВП: флурбипрофен, ацетиламинонитропропоксибензол, бензидамин.
Антиоксиданты
Антиоксиданты при лечении боли в горле применяются для улучшения метаболизма, восстановления работы ферментных систем и уменьшения разрушительного действия свободных радикалов и перекисных соединений, а также для повышения иммунитета (рутинсодержащие комплексы, витамины группы А, Е, С, микроэлементы Zn, Mg, Si, Fe, Ca, биодобавки, и др.).
Критерии эффективности лечения
Показателями того, что проводимое лечение обладает достаточной эффективностью, являются:
Но даже в этом случае курсы лечения лучше проводить не менее трех раз в год, особенно в период межсезонья.
Однако если у больного даже с простой формой хронического тонзиллита или ТАФ I возникает рецидив, то после первого курса лечения в небных миндалинах сохраняется гной, происходит образование казеозных масс, поэтому необходимо обсудить с пациентом возможность проведения тонзиллэктомии.
Таким образом, консервативное лечение хронического тонзиллита должно в какой-то мере рассматриваться как этап подготовки больного к тонзиллэктомии при хроническом тонзиллите ТАФ I, а при простой форме (при наличии положительного результата лечения) нужно научить пациента поддерживать миндалины в удовлетворительном состоянии – то есть проводить профилактику хронического тонзиллита. Многих интересует, как вылечить хронический тонзиллит раз и навсегда. К сожалению, универсальных рецептов для лечения хронического тонзиллита нет, так как это очаговая инфекция, которая постоянно снижает иммунитет и в любой момент может вызвать обострение состояния больного.
Таблица 1. Список лекарственных препаратов для лечения хронического тонзиллита у взрослых и детей (группа Rx)
| Время проведения бронхоальвеолярного лаважа после последней дозы, ч | Плазма | Альвеолярная жидкость | Альвеолярные макрофаги |
| 4 | 2,00±0,6 | 34,5±29 | 480±533 |
| 8 | 1,55±0,4 | 26,1±7 | 220±86 |
| 12 | 1,22±0,3 | 15,1±11 | 181±79 |
| 24 | 0,23±0,1 | 4,6±3 | 99,4±50 |
Тканевое накопление кларитромицина обеспечивает постоянное присутствие препарата в высоких концентрациях в очаге инфекции во время интервала между его приемами и некоторое время после окончания курса лечения (табл. 1). Это также позволило получить хорошие терапевтические результаты при попытке принимать кларитромицин 1 раз в день и укороченным курсом [52-54,73, 74, 78].
Выведение кларитромицина осуществляется печенью, почками и трансинтестинальным путем. При почечной недостаточности необходимо снижать дозу препарата. При печеночной недостаточности дозу уменьшать не следует [41].
Применяемая в педиатрии суспензия кларитромицина не имеет существенных отличий по фармакокинетическим характеристикам от таблетированной формы препарата. После приема суспензии образуется несколько меньшее количество метаболита 14-гидроксикларитромицина, но средняя сывороточная концентрация препарата выше [36].
Резистентность и фармакокинетика
При лечении инфекционного процесса антибиотики воздействуют не только на непосредственных возбудителей, но и на все чувствительные микроорганизмы микрофлоры. При этом возможна селекция резистентных штаммов и флора становится резервуаром для устойчивых микроорганизмов и детерминант резистентности. Это может затруднить лечение инфекций у пациента в будущем. Длительное действие препарата способствует развитию резистентности, особенно если концентрации антибиотика на слизистых оболочках долго держатся на субингибиторном уровне [3]. Это наиболее важно для макролидов, так как резистентность к ним развивается быстро и нерациональное их применение сегодня может сделать эти хорошие препараты неэффективными в дальнейшем [20].
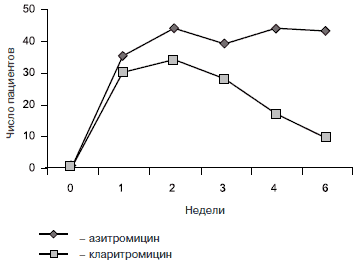
ALeach сообщает о том, что дети с трахомой через 2 мес после успешного лечения азитромицином были колонизированы азитромицин-резистентным S. pneumoniae в 21% случаев, тогда как до лечения только в 1,3% [2].
Частота выявления штаммов бактерий, резистентных к макролидам, после лечения азитромицином и кларитромицином [18].
Для снижения развития резистентности следует выбирать препараты, которые наименьшим образом воздействуют на естественную микрофлору человека, а также назначать адекватную суточную дозу и режим применения. Из антибиотиков группы новых макролидов наиболее щадящей фармакокинетикой обладает кларитромицин, который значительно меньше способствует селекции резистентности, чем азитромицин.
Кларитромицин при лечении инфекций нижних дыхательных путей у детей
Долгое время основными возбудителями инфекций нижних дыхательных путей у детей были пневмококк и гемофильная палочка и традиционные препараты вполне справлялись с этими возбудителями. В настоящее время эти бактерии остаются основными возбудителями пневмоний у новорожденных [40]. В последнее десятилетие на фоне неуклонного роста резистентности стрептококков, стафилококков и других возбудителей к препаратам пенициллинового ряда и другим широко применяемым антибиотикам наблюдается усиление значимости атипичных возбудителей, к которым относят хламидии, микоплазмы, легионеллы. Частота пневмоний, вызванных этими внутриклеточными возбудителями, постоянно увеличивается и в настоящее время варьирует в пределах 5-30%. Наиболее характерны атипичные пневмонии для детей школьного возраста [40, 52].
Кроме того, все чаще пневмония становится смешанной инфекцией, в которой могут одновременно участвовать и традиционные бактерии, и внутриклеточные микроорганизмы, и даже анаэробы. Участие нескольких возбудителей при достаточной тщательности исследования встречается почти в 1/2 случаев [24].
В этих условиях для лечения инфекций нижних дыхательных путей должны применяться препараты, обладающие активностью против всех наиболее вероятных возбудителей: стрептококков, пневмококков, стафилококков, гемофильной палочки, моракселлы, хламидий, микоплазм, легионелл, анаэробов. Кларитромицин обладает такой активностью, не уступает традиционным препаратам, а нередко и превосходит их по эффективности и имеет хорошую переносимость. Кларитромицин можно рекомендовать как препарат первого выбора для лечения внебольничных инфекций нижних дыхательных путей у детей [20, 40, 41, 46, 48, 52].
По сравнению с эритромицином кларитромицин показывает сходную эффективность, но наблюдается значительно меньше нежелательных явлений [41]. Так, в многоцентровом рандомизированном двойном слепом исследовании сравнивали эритромицин и кларитромицин при лечении пневмоний у 268 подростков [47]. Клиническая, рентгенологическая и микробиологическая эффективность препаратов была одинакова как для типичных, так и для атипичных пневмоний и составила 97% для кларитромицина и 96% для эритромицина. Однако пациенты, получавшие эритромицин, в 2 раза чаще страдали от побочных эффектов со стороны ЖКТ и в 5 раз чаще вынуждены были прервать лечение препаратом.
По клинической эффективности при лечении инфекций дыхательных путей между эритромицином и новыми макролидами нет значимых различий. Новые макролиды имеют преимущество как препараты со значительно лучшей переносимостью и более удобным режимом приема, что особенно важно для детей.
По эффективности кларитромицин не уступает не только другим макролидам, но также цефалоспоринам I и II поколений, защищенным и незащищенным пенициллинам 42. Более того, по активности против стафилококков, пневмококков и гемофильной палочки он может превосходить такие широко применяемые при лечении респираторных инфекций антибиотики, как рокситромицин, цефаклор и амоксициллин [29].
Некоторые авторы отмечают, что основные симптомы заболевания исчезают значительно быстрее при лечении кларитромицином, чем другими макролидами, а также фторхинолонами, пенициллином, амоксициллином и цефалоспоринами [28]. Возможно, это связано с высокой степенью антибактериальной активности кларитромицина. Данный факт имеет фармакоэкономическое значение, так как уменьшает затраты на симптоматическую терапию.
В последнее время появились сообщения, свидетельствующие о связи между бронхиальной астмой и инфицированием Chlamydiapneumoniae. Так, в работе U.Emre и соавт. у 11% детей с приступом удушья были обнаружены антитела к этому внутриклеточному возбудителю [43]. У 75% детей после эрадикации хламидий эритромицином или кларитромицином отмечали улучшение состояния по данным клинического и лабораторного обследования. Авторы предлагают включить макролиды в курс терапии детей с приступом бронхиальной астмы.
Кларитромицин при лечении ангин у детей
По данным крупного европейского многоцентрового исследования, при лечении тонзиллита или фарингита у 1065 детей кларитромицин был эффективен в 95% случаев [25].
Так, J.Still и соавт. провели рандомизированное исследование с участием 367 детей, страдающих стрептококковым, серологически подтвержденным фарингитом. В работе сравнивалась эффективность кларитромицина и пенициллина V. Оба препарата были высокоэффективны клинически, но по частоте эрадикации, исследуемой на 10-й день после окончания лечения, кларитромицин достоверно был эффективнее. Клиническое излечение в группе кларитромицина наблюдалось в 96%, а в группе пенициллина в 94% случаев. Эрадикация стрептококка была достигнута в 92 и 81% случаев соответственно [56]. Похожие данные, свидетельствующие о равной клинической эффективности макролида и пенициллина, но о лучшей эрадикации возбудителя в группе кларитромицина, были получены в другом контролируемом исследовании [63]. Более полная эрадикация в группе кларитромицина может быть связана с тем, что макролиды не разрушаются β-лактамазами стафилококков, гемофильных палочек и моракселл, присутствующих в ротоглотке, как это нередко происходит с препаратами пенициллинового ряда, когда стрептококк in vitro проявляет чувствительность, а эффективность in vivo существенно меньше из-за резистентной β-лактамазапродуцирующей сопутствующей микрофлоры и полной эрадикации не наблюдается [60].
Данные об одинаково высокой клинической (98 и 97% соответственно) и бактериологической (86 и 88% соответственно) эффективности кларитромицина и амоксициллина при тонзиллофарингите были получены в контролируемом британском исследовании с участием 191 ребенка [62].
Так, при сравнении кларитромицина, назначаемого в стандартной дозе в течение 5 дней, и 10-дневного курса терапии пенициллином оба препарата были высокоэффективны клинически, но частота эрадикации была значительно выше при применении кларитромицина (94 и 78% соответственно) [74].
В некоторых районах России встречаемость штаммов стрептококков, резистентных к эритромицину и другим макролидам, среди детей и взрослых достигает 13% [6]. По данным испанских педиатров, резистентные к кларитромицину штаммы были обнаружены в 7,8% из 750 наблюдений [55], в то же время в США, по данным широкомасштабного исследования, среди 700 детей резистентность пиогенного стрептококка к кларитромицину составляет меньше 2% и не является значимой клинической проблемой [58]. Ввиду быстрого развития резистентности повторное лечение макролидами в случае рецидива нежелательно, а первичное лечение лучше проводить кларитромицином, так как он благодаря своим фармакокинетическим способностям меньше способствует индукции резистентности.
Кларитромицин при лечении среднего отита у детей
При остром среднем отите макролиды можно использовать в качестве хорошей альтернативы к аминопени-циллинам и котримоксазолу, фармакокинетика которых не позволяет достигать высоких концентраций в полости среднего уха, тогда как кларитромицин обладает способностью накапливаться в очаге воспаления. Так, концентрация препарата в жидкости среднего уха у детей, страдающих острым средним отитом, была в 3-5 раз выше, чем в плазме крови [67]. Кроме того, β-лактамные антибиотики (пенициллины, цефалоспорины) могут разрушаться β-лактамазами пенициллин-резистентных штаммов пиогенного стрептококка и гемофильной палочки, которые получают все большее распространение [68, 69]. β-Лактамазы могут вырабатывать также другие бактерии, составляющие микрофлору носоглотки [68]. В России высока резистентность к котримоксазолу, поэтому макролиды можно рекомендовать использовать не как альтернативные препараты, а как лекарственные средства первого выбора и наибольшее предпочтение имеют новые макролиды, особенно кларитромицин [69].
По данным ряда многоцентровых исследований, суспензия кларитромицина высокоэффективна при среднем отите у детей. В германском исследовании с участием 102 пациентов на 5-й день терапии кларитромицином клиническое излечение было достигнуто в 99% случаев [66]. Побочные эффекты наблюдались у 3% детей. В испанском исследовании эффективности кларитромицина при респираторных инфекциях у детей [25] участвовали 310 больных острым средним отитом. Препарат показал свою эффективность в 96,1% случаев.
В большом количестве контролируемых сравнительных исследований было показано, что кларитромицин не уступает защищенным и незащищенным пенициллинам, цефалоспоринам, другим новым макролидам, а нередко и превосходит некоторые препараты, особенно пенициллины, по эффективности или безопасности 71.
Так, в рандомизированной работе с участием 736 детей кларитромицин показал одинаковую эффективность с амоксициллином/клавуланатом и цефаклором. При этом частота побочных эффектов у кларитромицина была в 2 раза меньше, чем в группе получавших амоксициллин/клавуланат, и составила 16% (36/221) для кларитромицина и 30% (74/244) для защищенного пенициллина [71].
При рандомизированном сравнении [70] суспензий кларитромицина и амоксициллина отдаленный эффект клинического излечения был получен в группе кларитромицина у 95% (20/21) детей, а в группе амоксициллина у 86% (19/22). Частота побочных эффектов не различалась и составила по 1 ребенку в каждой группе, но если в группе макролида тяжесть нежелательных явлений позволила продолжить лечение, то ребенок, получавший амоксициллин, был вынужден прервать терапию.
В слепом рандомизированном сравнительном исследовании кларитромицина и цефуроксима аксетила оказалось, что препараты одинаково высокоэффективны при лечении среднего отита, хорошо переносятся детьми и не различаются по частоте развития побочных эффектов [72].
Обычный курс лечения острого среднего отита составляет 10 дней. Более короткий 5-дневный курс терапии оказался не менее эффективным и более удобным для пациента [73, 75]. В рандомизированном слепом плацебо-контролируемом исследовании с участием 138 детей было показано, что назначение кларитромицина в течение 5 дней также эффективно и безопасно, как и 10-дневный курс лечения [75]. При сравнении кларитромицина и азитромицина, назначаемых в течение 5 дней, оба препарата были одинаково эффективны в 99% случаев при лечении детей со средним отитом; не различались они и по частоте нежелательных явлений.
Риносинуситы
Кларитромицин высокоактивен против основных возбудителей синуситов у детей и превосходит эритромицин по активности против гемофильной палочки. Кроме того, кларитромицин хорошо проникает в слизистую пазух носа и накапливается в них в концентрациях, превышающих сывороточные и минимальные подавляющие концентрации для возбудителей синусита [8, 79].
Контролируемых сравнительных исследований эффективности кларитромицина при синуситах у детей не проводилось. Однако на основании многоцентровых слепых рандомизированных сравнительных исследований, проведенных с участием взрослых, можно утверждать, что кларитромицин сопоставим по эффективности с ципрофлоксацином [82], левофлоксацином [80] и азитромицином [81].
Коклюш
У детей с коклюшем макролиды хотя и не влияют на продолжительность заболевания, но уменьшают тяжесть его клинических проявлений и вызывают быструю эрадикацию Bordetella pertussis из носоглотки [52, 76]. По этой причине макролиды, в том числе кларитромицин, могут применяться как препараты выбора для лечения коклюша у детей, а также для профилактического лечения членов семьи больного [77].
Обычно рекомендуемый курс лечения эритромицином составляет 12 дней. Однако благодаря улучшенным фармакокинетическим характеристикам новые макролиды, кларитромицин и азитромицин, могут применяться в течение 7 дней. Показано, что эффективность терапии при этом не уменьшается [78].
Дозировка
В последнее время, учитывая, что концентрации препарата в очаге воспаления намного превышают сывороточные, все чаще начинают говорить о возможности применения суточной дозы препарата однократно и о более коротком курсе терапии [41, 34]. В рандомизированном перекрестном исследовании на добровольцах было показано, что при назначении кларитромицина 1 раз в день в суточной дозе 500 мг или 2 раза в день в дозе 250 мг форма фармакокинетической кривой была одинакова [52]. При назначении 1 раз в день в тканях легкого высокие концентрации препарата сохранялись постоянно. Концентрация в альвеолярной жидкости превышала минимальную подавляющую для типичных бактериальных патогенов инфекций дыхательных путей, а концентрация в альвеолярных макрофагах превышала минимальную подавляющую концентрацию для важнейших внутриклеточных возбудителей. Таким образом, появились теоретические предпосылки для применения кларитромицина 1 раз в день, которые уже получили клиническое подтверждение.
Так, в двойном слепом рандомизированном многоцентровом исследовании эффективность кларитромицина, применяемого 2 или 1 раз в день, была одинакова при лечении обострения хронического бронхита у 265 взрослых пациентов [52]. Одинаковой также была частота побочных эффектов в целом, хотя нежелательные явления со стороны ЖКТ чаще наблюдались у получавших кларитромицин 2 раза в день.
При инфекциях дыхательных путей, особенно при тяжелых пневмониях, требующих стационарной терапии, может потребоваться внутривенное введение макролидов. К сожалению, до последнего времени парентеральные формы макролидов отсутствовали на российском рынке. У кларитромицина есть внутривенная форма, и она доступна в России.
При лечении инфекций дыхательных путей в стационаре в настоящее время популярна так называемая ступенчатая терапия, когда лечение начинается с внутривенного введения препарата, а затем через 1-3 дня переходят на пероральную форму того же лекарственного средства. Этим обеспечивается и больший комфорт для пациента, и меньше сил и средств затрачивается на лечение при равной эффективности. Благодаря наличию внутривенной формы и суспензии для перорального приема ступенчатую терапию можно использовать при лечении кларитромицином. В многоцентровом исследовании сравнивали кларитромицин и комбинацию цефуроксима и эритромицина при ступенчатой терапии внебольничных пневмоний у 235 пациентов [51]. Значимых различий между группами по частоте клинической или бактериологической эффективности не отмечено, тогда как нежелательных явлений (тошнота, рвота, диарея, боль в животе) было значительно больше среди получавших цефуроксим и эритромицин.
Переносимость и лекарственные взаимодействия
В целом макролиды, особенно представители нового поколения, относятся к препаратам с благоприятным профилем безопасности и хорошо переносятся детьми. Наиболее характерны для детей при приеме кларитромицина нежелательные явления со стороны ЖКТ, такие как тошнота (1%), рвота (6%), диарея (7%), боли в животе (2%) и головные боли (2%). Реже встречаются аллергические реакции, симптомы гепато- и ототоксичности, нежелательные явления со стороны нервной системы [65]. В целом нежелательные явления у эритромицина, кларитромицина и азитромицина не намного различаются и наблюдаются в 4-27% случаев [64]. Это сопоставимо с частотой побочных эффектов, наблюдающихся при приеме детьми суспензий β-лактамных антибиотиков (ампициллина, ампициллина/клавуланата, цефаклора и др.) [65].
Активное использование макролидов в последние годы и расширяющаяся полипрагмазия увеличили вероятность развития лекарственных взаимодействий с препаратами, подвергающимися инактивации системой микросомальных ферментов цитохрома P-450. Поскольку метаболизация кларитромицина осуществляется микросомальными ферментами печени с участием системы цитохрома P-450, то кларитромицин может оказывать влияние на метаболизм всех препаратов, проходящих через эту систему [41]. При этом кларитромицин обладает меньшей способностью, чем эритромицин, увеличивать концентрации в сыворотке таких препаратов, как циклоспорин, варфарин, теофиллин, карбамазепин, терфенадин, но совместное назначение кларитромицина с последними тремя лекарственными средствами противопоказано [64].
Заключение
В настоящее время не утихли споры относительно сравнения преимуществ и недостатков эритромицина и новых макролидов. Еще сложнее разобраться в различиях между наиболее удачными новыми макролидами, азитромицином и кларитромицином [49]. Несмотря на равную клиническую эффективность при лечении инфекций дыхательных путей и мягких тканей, эти препараты имеют существенные различия по таким показателям, как фармакокинетические характеристики, профиль безопасности, комплаентность, частота эрадикации, которые нередко недооцениваются, хотя их необходимо учитывать (табл. 2).
Таблица 2. Сравнительная характеристика эритромицина и кларитромицина
| Показатель | Эритромицин | Кларитромицин |
| Активность против гемофильной палочки | 0 | ++ |
| Активность против стафилококков, пневмококков, стрептококков, хламидий | + | ++ |
| Независимость от приема пищи | 0 | + |
| Активность метаболита | 0 | + |
| Накопление в очаге воспаления | 0 | + |
| Противовоспалительная активность | 0 | + |
| Частота приема | 4 раза в сутки | 2 раза в сутки |
| Нежелательные явления | ++ | + |
| Лекарственные взаимодействия | ++ | + |
В настоящее время выбор эмпирической терапии инфекций у детей должен основываться на таких свойствах препаратов, как эффективность, безопасность (нежелательные явления), комплаентность (возможность перорального применения, независимость от приема пищи, назначение 1-2 раза в день, приятный вкус, короткий курс терапии) [45, 48].
Кларитромицин обладает почти всеми характеристиками идеального антибиотика для лечения респираторных инфекций у детей [7, 8]: высокая биодоступность при пероральном применении, высокая эффективность при относительно низких дозах препарата, длительный интервал между приемами, сбалансированная концентрация в тканях и крови, высокая внутриклеточная концентрация, высокая активность основных метаболитов, широкий спектр антибактериальной активности, включающий всех основных возбудителей инфекций дыхательных путей, и, наконец, безопасность и хорошая переносимость.