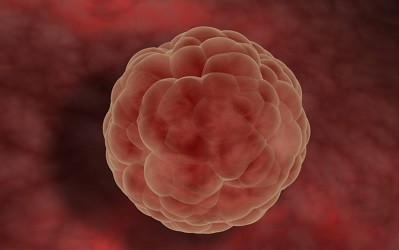
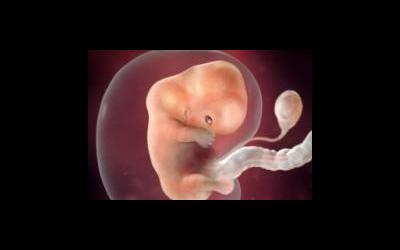
8 факторов, способствующих имплантации эмбриона
Часто, несмотря на создание генетически нормальных эмбрионов, после их перенесения в матку, беременность не наступает.
Так что же влияет на их имплантацию?
Не должно быть никаких структурных препятствий для имплантации, таких как аномалии матки, полипы, миомы, остаточные продукты более раннего выкидыша или аденомиоза. Некоторые из этих препятствий могут потребовать хирургическое вмешательство.
Приток крови к матке, и особенно к эндометрию, выгоден для имплантации.
Частота маточных сокращений увеличивается примерно во время овуляции и обычно успокаивается ко времени имплантации примерно через 5-6 дней. Однако нет ничего необычного в том, что женщины, перенесшие эмбрион в цикле ЭКО, испытывают некоторые судороги. Чем больше сокращений после переноса эмбриона, тем ниже вероятность успешной имплантации.
Исследования показали, что для успешной имплантации оболочка должна быть не менее 6 миллиметров. Это требует правильной структуры тканей, правильных рецепторов и правильного баланса гормонов.
Нужен хороший уровень эстрогена, чтобы восполнить и стимулировать рост восприимчивой оболочки, и прогестерона, чтобы ослаблять сократительную способность матки во время имплантационного периода. В некоторых циклах ЭКО уровни этих гормонов не идеальны и не имеют ничего общего с теми уровнями, которые организм испытывает в нормальном менструальном цикле. Вот почему некоторые клиники ЭКО, в том числе и мы, предпочитают переносить эмбрионы в естественном цикле.
Повышенный уровень определенных иммунных клеток матки, называемых естественными киллерами, препятствует успешной имплантации. С другой стороны, действия некоторых Т-клеток и NK-клеток необходимы для создания благоприятной среды для имплантации. Здесь должен быть баланс.
Женщины, которые питаются преимущественно свежими овощами, фруктами, рыбой, имеют более благоприятный аминокислотный профиль в матке, чем женщины, которые едят много мяса и молочных продуктов. Считается, что это может поддерживать развитие и имплантацию эмбрионов.
Имплантация эмбриона: основные симптомы и ощущения после прикрепления плодного яйца
Немного теории
Внедрение плодного яйца в матку называется имплантацией. Ворсинки эмбриона проникают в слизистую оболочку матки, что может быть причиной незначительного кровотечения.
Для того чтобы имплантация прошла успешно, нужно соблюдение сразу нескольких условий:
Сроки имплантации
Условно можно выделить среднюю, позднюю и раннюю имплантации.
Если беременность не наступает длительное время, то нужно обследоваться для выявления причины бесплодия.
Субъективные и объективные признаки
При этом следует различать уровни болей, обильность и насыщенность выделений, повышение температуры тела. Иногда то, что выдается за имплантацию плодного яйца признаки, является симптомами какого-то другого заболевания. Если вы сомневаетесь, являются ли ваши ощущения 5 дпо признаками имплантации плода или нет, лучше обратиться к врачу.
Развитие эмбриона по дням после ЭКО
Если с естественным циклом все более или менее понятно, то вопрос, на какой день происходит имплантация эмбриона в удачном протоколе остается открытым. Предлагаем вашему вниманию табличку по дням:
Примерно на 11 день (11-12 ДПП) после переноса можно делать выводы о том, было ли удачное ЭКО.
Доверяем природе
Женщины перечитывают тонны литературы, стремясь найти те самые 5 дпо ощущения или 6 дпп ощущения, которые указывали бы на имплантацию и соответственно наступление беременности. Собственно, переживать, получилось или нет, будущие мамы начинают еще на 3 ДПО.
Вопрос этот одинаково волнует и девушек, прошедших процедуру ЭКО. Предполагаемую имплантацию эмбриона после ЭКО стараются уловить по минимальным изменениям в организме и самочувствии. Интернет пестрит запросами, вроде «5 дпп трехдневок», «4 дпп пятидневок», «7 дпп пятидневок», с помощью которых женщины ищут положительные истории.
Горьким разочарованием становится отсутствие даже намека на вторую полосу на 8 день или месячные после переноса эмбрионов. А ведь на самом деле, ответом на вопрос о том, почему не приживается эмбрион, может быть объективная ситуация естественного отбора. Нежизнеспособный плод был отторгнут, дав дорогу здоровому потомству.
Справедливости ради стоит отметить, что если такое отторжение повторяется постоянно, то это повод для проведения полного медицинского обследования. Причиной ненаступления долгожданной беременности может быть имужское бесплодие.
Прикрепление плодного яйца к матке
Содержание
Прикрепление плодного яйца осуществляется после 4-5 дней после попадания сперматозоида в организм женщины. Еще сутки или двое нужны, чтобы оно закрепилось на своем месте. После этого начинается активная фаза роста гормона ХГЧ, который сможет безошибочно подтвердить или нет ваше интересное положение.
Симптомы прикрепления плодного яйца
Само внедрение возможно лишь в определенные дни цикла, это связано с процессом овуляции. Все эти данные обязательно берутся во внимании при планировании искусственного оплодотворения. Увидеть эмбрион еще не возможно, но, сдав анализ на рост гормона ХГЧ, вы сможете с точностью определить, беременны вы или нет. А уже через 1-2 недели тест покажет долгожданные для многих две полоски. Важно отметить, что никаких явных симптомов прикрепления плодного яйца к матке нет. Хотя некоторые женщины отмечают у себя покалывание внизу живота, ноющие боли, боли в пояснице, слабость, тяжесть в матке и т.д. Это все можно считать индивидуальными проявлениями, но никак не правилом. Ощутить это практически невозможно, с точки зрения медицины это никак не подтверждается. Так как процесс происходит на микроскопическом уровне и не сопровождается интенсивными проявлениями со стороны организма женщины. Достаточно редким симптомом прикрепления плодного яйца к матке являются небольшие выделения, которые зачастую вызывают беспокойство у врачей, так как могут свидетельствовать и о других заболеваниях и нуждаются в тщательном осмотре специалиста.
Прикрепление плодного яйца к матке
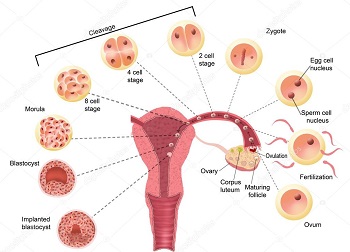
Выделения при прикреплении плодного яйца
Считается нормой возможные небольшие выделения при прикреплении плодного яйца к матке. Такое встречается не у всех женщин и является скорее исключением из правил, нежели точным признаком долгожданной беременности. Особое внимание нужно обратить на объем и цвет выделений. Если это действительно выделения связанные с процессом имплантации, то их количество должно составлять не более нескольких капель в течение одного дня, без всяких сгустков крови. Цвет выделений может быть красным, светло-желтым, коричневым или розовым. Чаще всего выделения наблюдаются на 7-8 день после попадания сперматозоида в матку. Но это данные достаточно субъективные и зависят от индивидуальных особенностей каждой женщины.
Если вы заметили, что выделений стало больше и они красного цвета, следует немедленно обратиться к врачу. Это могут быть признаки угрозы выкидыша или маточного кровотечения. В таком случае будет важна каждая минута, ведь от этого будет зависеть жизнь вашего малыша и вас самой. Кроме того такие выделения могут стать первыми признаками более серьезных заболеваний, к которым относятся онкологические заболевания, гормональные сбои, доброкачественные опухоли, отслоение или воспаление эндометрия, эрозии, цервициты и т.д. Только специалист после тщательного осмотра сможет поставить точный диагноз и назначить правильное лечение. Поэтому не забывайте регулярно посещать врача и сдавать соответствующие анализы.
Что влияет на успех имплантации
Еще планируя беременность, следует учитывать продолжительность приема гормональных препаратов и длительность использования внутриматочной спирали. Все эти факторы делают внутреннюю слизистую матки недостаточно чувствительной, в результате чего может развиться плацентация или шеечная беременность. Не забывайте также о вредных привычках. Откажитесь от употребления спиртных напитков и курения. Старайтесь больше проводить времени на свежем воздухе, в еде отдайте предпочтение нежирным сортам мяса и рыбы, свежим овощам и фруктам, которые богаты на витамины и минералы естественного происхождения. Избегайте контакта с вредными веществами, а также, если вы принимаете какие-то препараты, проконсультируйтесь с врачом об их побочных эффектах.
Прикрепление плодного яйца к полости матки – один из важнейших этапов в развитии эмбриона. От того, как будет происходить этот процесс, зависит дальнейшей развитие или неразвитее беременности. Поэтому важно прислушиваться к советам гинеколога и тогда через 9 месяцев у вас будет здоровый и крепкий малыш.
Самые важные и интересные новости о лечении бесплодия и ЭКО теперь и в нашем Telegram-канале @probirka_forum Присоединяйтесь!
Имплантация плодного яйца: ощущения, симптомы
Имплантация плодного яйца – это самое начало периода беременности. Он практически не ощутим будущей мамой, но, тем не менее, невероятно важен для развития ребенка. Его важность подтверждается тем, что если плодное яйцо не будет имплантировано – ребенка просто не получится.
В данной статье мы рассмотрим симптомы имплантации плодного яйца, его сроки и ощущения, которые может испытывать женщина. Многие ученые утверждают, что впервые женщина чувствует что-то уже после имплантации, тем не менее, выделения при имплантации плодного яйца могут сказать о многом.
Когда происходит имплантация плодного яйца: сроки
Имплантация плодного яйца – день, в который яйцеклетка прикрепляется в матке. Это, как правило, происходит спустя четверо суток после успешного секса. Сам период прикрепления занимает около 48 часов.
Именно в это время организм начинает вырабатывать гормон ХГЧ. Таким образом, уже через полторы недели вы сможете сделать тест и узнать о возможной беременности. И совсем не надо ждать мифических признаков имплантации плодного яйца.
Однако необходимо помнить, что наилучший результат даст анализ крови, который можно сдать в любом платном клиническом кабинете.
Симптомы имплантации плодного яйца
Да, многие врачи утверждают, что боли при имплантации плодного яйца просто невозможны и не могут тревожить ни одну из женщин, так как все это происходит на уровне клеток и размеры плодного яйца минимальны. Тем не менее, многие женщины утверждают, что чувствовали тянущие ощущения внизу живота, да и природа их совсем непонятна.
Что касается выделений при имплантации плодного яйца, то тут совсем другое дело. Это могут быть скудные (и только такие) выделения с небольшими примесями крови. В противном случае, причина появления таких симптомов может быть тревожной. Так, кровотечения и другие выделения в середине менструального цикла могут свидетельствовать не об имплантации плодного яйца, а об ухудшении физического состояния женщины.
Так что, если говорить про ощущения при имплантации плодного яйца, то можно утверждать, что этот момент проходит бесследно для большинства женщин. При этом стоит помнить, что имплантация плодного яйца, признаки которой слишком явные для женщины, скорее всего, говорят о том, что она прошла неудачно, и стоит показаться врачу.
Обзор процесса имплантации плодного яйца
Итак, что чувствует женщина, какие выделения при имплантации плодного яйца у нее могут быть, описано. Теперь можно перейти к «взгляду изнутри». А именно рассмотреть, как в это время ведет себя яйцеклетка.
Яйцеклетка начинает движение по направлению к матке. В это время она все еще продолжает делиться. Врачи в этот период называют ее уже не яйцеклеткой, а морулой. На этот момент она состоит из тридцати двух клеток и внешне чем-то напоминает малину.
Трое суток яйцеклетка двигалась в матку, а затем еще столько же она продолжает движение до места прикрепления. К моменту шестых суток морула становится бластоцистой. В этот момент в ней двести пятьдесят клеток и ее размеры уже полтора миллиметра. Она уже состоит из двух слоев – ворсистой поверхности (трофобласта) и самого зародыша (эмбриобласта). Температура при имплантации плодного яйца не должна превышать норму. Поэтому, если женщина планирует стать матерью, ей не рекомендуется принимать очень горячие ванны. Ворсинки помогают зародышу сливаться с организмом матери. А весь процесс занимает не менее сорока часов.
Впервые рассмотреть будущего малыша можно через три-четыре недели после имплантации плодного яйца. В это время он достигает размеров около сантиметра.
Иммунология имплантации.
Когда попытка добиться беременности с помощью оплодотворения in vitro не удается, мы часто не можем объяснить причину этого. Эта статья обращается к вопросу несостоятельности имплантации и роли иммунной системы в достижении успешной беременности. Какие методы обследования могут помочь установить причину неудачи, и что мы делаем, если обнаруживаем нарушения? Выступление доктора Каролины Кулам (Carolyn B. Coulam), одного из ведущих специалистов в области иммунологии репродукции, на 8-й конференции по оплодотворению in vitro в 1995 г. было посвящено этой проблеме.
Введение
В течение почти 20 лет применяется и развивается оплодотворение in vitro (IVF) и перенос эмбриона (ET). Но несмотря на технологические успехи, ведущие к повышению частоты зачатий, частота наступления имплантации при подсадке зародышей заметно не улучшилась и остается между 10 и 15%. Поэтому именно наступление или ненаступление имплантации отличает успешный цикл IVF от безуспешного, и частота безуспешных циклов при IVF составляет 70-80%. Неудачная имплантация может быть следствием либо аномалий зародыша либо аномалий эндометрия. По некоторым оценкам, частота зародышей с аномалиями хромосомного набора, доступных для имплантации, составляет 30-80%. Если вероятность получения аномального зародыша в результате IVF составляет 60%, а в полость матки переносится 3 зародыша, вероятность того, что хотя бы один зародыш окажется с нормальным хромосомным набором составляет 78%. Но почему же тогда частота наступления беременности в результате IVF составляет 30%? Определенное значение в этом могут иметь аномалии эндометрия (слизистой оболочки матки). Низкая частота имплантации и наступления беременности после IVF стимулировала исследования, направленные на понимание механизмов имплантации в связи с рецептивностью эндометрия и взаимодействиями между зародышем и маткой. В следующих разделах сделан обзор результатов этих исследований и представлены клинические приложения диагностики и лечения нарушений имплантации.
Механизмы имплантации
Успешная имплантация требует наличия рецептивного эндометрия и нормальных взаимодействий между рецептивным эндометрием и зародышем.
Эндометрий состоит из железистого эпителия, стромы и лимфомиелоидных клеток. Для поддержки нормальной беременности, эндометрий должен дифференцироваться в децидуальную оболочку. У человека эндометрий превращается в децидуальную оболочку под действием гормонов, лимфоидных и трофобластных клеток. Любые события, которые могут повлиять на действие гормонов, лимфоидных или трофобластных клеток могут затормозить нормальное развитие децидуальной оболочки. Факторы, которые могут помешать децидуальной функции можно разделить на анатомические, гормональные и иммунные. К анатомическим дефектам, которым приписывается неблагоприятное влияние на децидуальную функцию, относятся полипы эндометрия, подслизистые узлы миомы и внутриматочные сращения. Вероятно, что дефекты Мюллеровых протоков (аномалии строения матки) не являются причиной выкидыша в первом триместре беременности. Гормональная недостаточность, связанная с выкидышем в первом триместре беременности, включает в себя недостаток прогестерона. В последние годы появились публикации, в которых рассматривается роль иммунной системы в успехе имплантации зародыша.
Во время имплантации клетки трофобласта обмениваются сигналами с клетками эндометрия и с лимфоидными клетками. Медиаторами этих сигналов являются цитокины и белки поверхности клеток. HLA-G, белок тканевой совместимости, экспрессируемый на поверхности клеток трофобласта, распознается лимфоцитами CD8+. Лимфоциты CD8+ секретируют цитокины, которые стимулируют рост и дифференцировку клеток трофобласта. По мере того как трофобластные клетки пролиферируют и проникают в эндометрий, они дифференцируются на внутренний слой цитотрофобласта и наружный слой синцитиотрофобласта. Все факторы, могущие помешать дифференцировке цитотрофобласта в синцитиотрофобласт, могут помешать нормальному развитию беременности. Было показано, что антифосфолипидные антитела (АФА) задерживают дифференцировку цитотрофобласта в синцитиотрофобласт, и их присутствие в сыворотке крови женщин связано с неблагоприятным исходом беременности.
Клетки трофобласта устойчивы к лизису цитотоксическими T-лимфоцитами и NK-клетками (естественными киллерами), но не резистентны к лизису активированными NK-клетками, или LAK-клетками (lymphocyte activated killer). Было показано, что целый ряд цитокинов подавляет активацию NK-клеток и их превращение LAK-клетки и предотвращает аборт у мышей. Этими цитокинами являются интерлейкин-3 (IL3), фактор, стимулирующий колониеобразование гранулоцитов и моноцитов (GM-CSF), фактор трансформации роста бета 2 (TGF-бета-2) и белок с молекулярной массой 34кДа, вырабатываемые клетками CD8+, имеющими рецепторы к прогестерону. Выработка этих цитокинов изучалась на местном уровне в области фетодецидуальной интерфазы, но есть данные, что имеется и системная активность данных факторов. На системном уровне данные факторы могут определяться в виде системных эмбриотоксинов с помощью теста на эмбриотоксичность. В крови можно определять и уровень NK-клеток (клеток CD56+). Повышение процента клеток CD56+ в крови был связано с ранним прерыванием кариотипически нормальной беременности. В связи с этим выявление повышенных концентраций в крови антифосфолипидов (а также других аутоантител, включая антитиреоидные и антиядерные антитела), повышенного процента клеток CD56+ и повышенного содержания эмбриотоксинов используется для выявление женщин, относящихся к группе риска наличия иммунологических факторов, способствующих неполноценной имплантации.
Диагностика неполноценной имплантации
Понимание механизма развития неполноценной имплантации позволяет применить более целенаправленный подход к выявлению факторов риска данного состояния. В настоящее время для выявления факторов риска используются определение в крови антифосфолипидных антител, процента циркулирующих клеток CD56+ и выявление циркулирующих эмбриотоксинов.
Для выяснения активности антифосфолипидных антител была проведена большая работа. Молекулы фосфолипидов выполняют адгезивную функцию при формировании синцитиотрофобласта. Иммуногенное состояние возникает при экспозиции поверхностных фосфолипидов (особенно фосфатидилсерина и фосфатидилэтаноламина в форме гексагональной фазы II). Антитела к этим фосфолипидам вмешиваются в процесс образования синцитиотрофобласта из цитотрофобласта, что ведет к задержке синцитиолизации цитотрофобласта. Данный механизм был предложен для объяснения патогенеза недостаточности имплантации. В настоящее время изучается роль других аутоантител в развитии неполноценной имплантации, включая антинуклеарные и антитиреоидные антитела.
Было показано, что моноциты децидуальной оболочки, которые имеют экспрессию CD56+, связаны с успехом имплантации. Дефицит естественных клеток-киллеров, имеющих фенотип CD56+, наблюдался в биоптатах из плацентарного ложа у женщин с угрожающим ранним выкидышем. Исследования на животных показали значение клеток CD56+ в предотвращении выкидыша через четыре дня после начала имплантации. В этой модели успех эмбрионального аллографта был связан с локальной суппрессии на уровне децидуальной оболочки факторами, выделяемыми клетками CD56+. В других исследованиях было высказано предположение, что для успеха репродуктивного процесса важна системная регуляция антитрофобластных клеток-киллеров. Было показано, что у женщин, страдающих привычным невынашиванием беременности, периферические NK-клетки участвуют в цитотоксических реакциях на трофобластные клетки собственных зародышей женщины.
Было показано, что концентрации циркулирующих клеток CD56+ коррелируют с успехом наступления беременности у бесплодных женщин. Процент циркулирующих клеток CD56+ больше 12 предсказывает отторжение кариотипически нормального зародыша со специфичностью 87% и с положительной предиктивной ценностью в 78%. Однако, хотя этот тест обладает высокой специфичностью, его чувствительность среди бесплодных женщин, которым проводится лечение вспомогательными методами репродукции, достаточно низка (54%), что указывает на то, что данное исследование не может выявить все периимплантационные потери среди данных супружеских пар (например, аномальные зародыши).
Целый ряд исследователей обнаружили эмбриотоксические факторы в крови женщин с репродуктивной недостаточностью. Было показано, что эти эмбриотоксины относятся как к высокомолекулярным (иммуноглобулины), так и к низкомолекулярным (цитокины) фракциям. В то время как в децидуальной ткани был выявлен широкий спектр растворимых медиаторов, способствующих имплантации, некоторые цитокины могут оказывать прямое или непрямое цитотоксическое действие на зародыш. Для выявления таких эмбриотоксинов был разработан специальный тест, использующий бластоцисты мыши. Этот тест прошел первые испытания и называется тестом на эмбриотоксичность.
Лечение неполноценной имплантации
Можно ожидать, что иммунотерапия может помочь повысить шансы рождения живого ребенка в случаях, когда иммунологические механизмы принимают участие генезе нарушения течения беременности. Однако иммунотерапия не может помочь в случаях, когда невынашивание связано с аномалиями зародыша. Это указывает на важность выявления именно тех пациенток, которым может помочь иммунотерапия. Понимание патогенетических механизмов нарушения имплантации позволяет применить сфокусированный подход к специфичности лечения. К тестам, которые могут быть использованы для выработки тактики лечения, относятся определение уровня антифосфолипидных антител, циркулирующих клеток CD56+ и циркулирующих эмбриотоксинов.
В недавнем исследовании Sher и сотр. сообщили, что АФА были обнаружены в крови 53% женщин с диагнозом органического заболевания таза, которым предполагалось проведение IVF. Назначение аспирина по 80 мг в день и гепарина по 5000 МЕ 2 раза в день значительно (p менее 0,05) улучшило частоту жизнеспособной беременности (49%) по сравнению с не леченной группой женщин с АФА (16%). Таким образом, у женщин с АФА, которым проводилось лечение методом IVF, было показано повышение частоты беременности на 33%.
Мы сравнили частоту положительного анализа на АФА у женщин с успешными и с безуспешными циклами IVF. Частота положительного анализа на АФА среди женщин с безуспешными циклами (26%) была значительно (p=0,007) выше, чем у женщин с успешными циклами (5%).
Недавние данные указывают, что лечение внутривенными иммуноглобулинами (IVIg) помогает удержать беременность у женщин с повышенным уровнем клеток CD56+ в крови. В данном исследовании 13 женщинам проводилось лечение IVIg и ни у одной из них не было выкидыша. Частота повышенных уровней циркулирующих клеток CD56+, связанных с исходом беременности у женщин, получавших и не получавших IVIg представлена в табл. 1. У женщин с уровнем CD56+ клеток выше 12%, частота благоприятного исхода беременности была значительно выше (p=0,0002) при назначении IVIg.
Эмбриотоксические факторы были выявлены в крови женщин с неудачными попытками IVF. Эти эмбриотоксические факторы могут вырабатываться активированными лимфоцитами после стимуляции трофобластом. Поскольку было показано, что лечение IVIg регулирует функцию как Т-, так и В-лимфоцитов, достаточно обосновано применение данного метода лечения у женщин с неполноценной имплантацией на фоне циркулирующих эмбриотоксинов. Лечение женщин с положительным тестом на эмбриотоксичность путем внутривенного введения иммуноглобулинов привело к рождению живых детей. Однако в этих исследованиях не было контрольных групп. Хотя резонно, что применение иммунотерапии, которая модулирует выработку цитокинов, должно быть эффективно для модулирования выработки цитокинов, проявляющих эмбриотоксическое действие, для уточнения эффективности иммунотерапии при привычном невынашивании беременности, связанном с циркулирующими эмбриотоксинами, требуются дальнейшие исследования.
После первых сообщений об успешной иммунотерапии постфертилизационной недостаточности (привычное невынашивание беременности), возник вопрос о возможности ее применения для лечения пре- и периимплантационной недостаточности. Постановка этого вопроса связана с наблюдением, что при имплантации важную роль играет воспалительная реакция. Факторы воспалительной реакции необходимы для успешной беременности. Некоторые из этих факторов имеются в плазме спермы. В исследованиях на животных было показано, что эти факторы потенцируют имплантацию. Но некоторые компоненты воспалительной реакции могут быть фатальны для беременности. Было показано, что некоторые заболевания, возникающие в результате воспалительных реакций, могут быть успешно лечены с помощью IVIg.
Сравнение частоты наступления беременности при применении инсеминации и при абстиненции в день переноса гамет у женщин, лечившихся от бесплодия с помощью IVF (53% против 23%) и GIFT (81% против 31%, p менее 0,01) показало благоприятное влияние инсеминации на исход лечения. В большом числе исследований на животных было показано, что это было связано не со сперматозоидами, а с фактором или с факторами плазмы спермы. Частота имплантации бластоцист у крысы на 4-й день псевдобеременности была значительно выше (91%) после инсеминации плазмы спермы, чем в контрольной группе (45%). В других исследованиях было показано, что частота имплантации у мышей, крыс и хомячков значительно снижается после хирургического удаления семенных пузырьков, но не после удаления вентральной части предстательной железы. Дальнейшие исследования на хомячках позволили предположить, что снижение процента имплантации после удаления семенных пузырьков является результатом более медленного деления клеток в процессе эмбрионального развития и гибелью зародышей. Удаление семенных пузырьков не влияло на частоту зачатий, а задержка делений наблюдалась через 72 часа после коитуса; имплантация происходила через 122 часа после коитуса.
В рандомизированном исследовании с использованием контрольной группы, в которой применялось плацебо, проводилось исследование влияния плазмы спермы на частоту имплантации. В исследовании участвовало 87 женщин, лечившихся по поводу бесплодия. 44 женщины получали влагалищные капсулы, содержащие плазму спермы, а 43 женщины получали плацебо на 7-й, 14-й и 21-й дни менструального цикла. У женщин, которые получали семенную плазму, ультразвуковое подтверждение имплантации наблюдалось чаще, чем у женщин, получавших плацебо (80% против 64%). Природа фактора или факторов плазмы спермы, потенцирующих имплантацию, пока не известна. Было показано, что имплантацию потенцируют такие факторы спермы, как полиамины, TGF-альфа и остеопонтин. После того как специфические усилители имплантации будут выделены из плазмы семени человека, они смогут быть использованы для лечения бесплодия, обусловленного постфертилизационной недостаточностью.
В нескольких исследованиях было показано повышение частоты имплантации по сравнению с применением плацебо у женщин, лечившихся по поводу бесплодия методом IVF, которым проводилось внутривенное введение иммуноглобулинов. Для ответа на вопрос о том, каким женщинам целесообразнее всего проводить лечение иммуноглобулинами было проведено исследование, в котором приняли участие женщины, у которых беременность не наступила после переноса в полость матки не менее 12 зародышей. Была выделена группа женщин, являвшихся эффективными производителями зародышей (более 50% оплодотворенных яйцеклеток и не менее 3-х зародышей, в каждом лечебном цикле). В данной группе беременность наступила у 56% пациенток. В группе неэффективных производителей частота наступления беременности составила всего лишь 5%. Частота имплантации составила 17% в группе эффективных производителей и 0% в группе неэффективных производителей (p=0,007). Частота живорождений на одну пациентку была существенно выше в группе эффективных производителей (44%), чем в группе неэффективных производителей (0%) (p=0,0002). Таким образом, вероятно, что усиление эффективности лечения бесплодия методом IVF с помощью IVIg наиболее вероятно у женщин, у которых в анамнезе был выкидыш кариотипически нормальным зародышем, выкидыши на доклинической стадии в анамнезе, у которых в процессе IVF оплодотворение наступает у более 50% яйцеклеток, и у которых в каждом цикле IVF образуется не менее трех зародышей.